Ioniske faste stoffer:Forståelse af ionarrangement i krystalgitter
* Ioniske forbindelser er lavet af kationer og anioner: En ionforbindelse består af positivt ladede ioner (kationer) og negativt ladede ioner (anioner).
* Alternative ioner: For at opretholde elektrisk neutralitet veksler disse ioner i krystalgitteret. Så ved et givet gitterpunkt kan du finde en kation, mens du ved det tilstødende gitterpunkt finder en anion.
* Forskellige størrelser: Kationer er typisk mindre end anioner. Denne forskel i størrelse kan påvirke, hvordan de pakker sig sammen i gitteret.
Eksempel:
I NaCl (bordsalt) er gitterpunkterne optaget af:
* Natriumioner (Na+)
* Chloridioner (Cl-)
De veksler for at skabe en stabil, gentagende struktur.
Nøgleafhentning: Mens ioniske faste stoffer har et præcist, gentaget arrangement, er selve gitterpunkterne optaget af forskellige typer ioner, ikke altid et enkelt atom.
Sidste artikelYttrium:Egenskaber, anvendelser og anvendelser i teknologi
Næste artikelForståelse af oxidationstilstanden for mangan (Mn₂)
 Varme artikler
Varme artikler
-
 Bare tilsæt vand - Kemikere afslører en mekanisme bag doping af organiske halvledereDenne Lewis-syre ændrer de elektriske egenskaber af visse organiske halvledere, når den tilsættes i tilstedeværelsen af vand Kredit: Brett Yurash Halvledere – og vores beherskelse af dem – har g
Bare tilsæt vand - Kemikere afslører en mekanisme bag doping af organiske halvledereDenne Lewis-syre ændrer de elektriske egenskaber af visse organiske halvledere, når den tilsættes i tilstedeværelsen af vand Kredit: Brett Yurash Halvledere – og vores beherskelse af dem – har g -
 Forskning fjerner kulden fra isdannelse på fly og vindmøllerUBCO-forsker Mohammad Zarifi har foretaget væsentlige forbedringer af realtidssensorerne, der overvåger frost- og isopbygning på fly og turbiner. Kredit:UBCO Ny UBC Okanagan-forskning ændrer den m
Forskning fjerner kulden fra isdannelse på fly og vindmøllerUBCO-forsker Mohammad Zarifi har foretaget væsentlige forbedringer af realtidssensorerne, der overvåger frost- og isopbygning på fly og turbiner. Kredit:UBCO Ny UBC Okanagan-forskning ændrer den m -
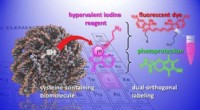 Nye kemiske værktøjer til at modificere og studere biomolekylerEn illustration af den kemiske reaktion udviklet i undersøgelsen. Kredit:J. Waser/B. Fierz (EPFL) Forståelse af strukturen og metabolismen af celler og levende organismer er afgørende for udvikl
Nye kemiske værktøjer til at modificere og studere biomolekylerEn illustration af den kemiske reaktion udviklet i undersøgelsen. Kredit:J. Waser/B. Fierz (EPFL) Forståelse af strukturen og metabolismen af celler og levende organismer er afgørende for udvikl -
 Fordampning vs. kogning:De to nøgleformer for fordampningAf John McDaniel , Opdateret 24. marts 2022 Fordampning er overgangen af en væske til en gas. I dagligdagens videnskab driver to primære mekanismer denne proces:fordampning og kogning. At forstå nuan
Fordampning vs. kogning:De to nøgleformer for fordampningAf John McDaniel , Opdateret 24. marts 2022 Fordampning er overgangen af en væske til en gas. I dagligdagens videnskab driver to primære mekanismer denne proces:fordampning og kogning. At forstå nuan
- Hvordan er de 3 former for stråling fra solen?
- Astronomer beskriver et voldsomt sort hul-udbrud, der giver ny indsigt i galaksehobens udvikling
- Hvad er mørkt inde, men let udenfor?
- Biologisk organisation:Fra celler til organsystemer forklaret
- Pandemic Moneyball:Hvordan COVID-19 har påvirket baseball odds
- Mandlige kunstnere dominerer gallerier. Er det fordi kvinder ikke maler særlig godt, eller bare dis…


