Forståelse af syre-base-indikatorer:Hvordan de virker og opdager syrer/alkalier
Sådan fungerer indikatorer:
1. Struktur og farve:
* Indikatorer er normalt svage organiske syrer eller baser.
* De findes i to former, hver med en særskilt farve:
* Syreform: Denne form foretrækkes i sure opløsninger og har én farve.
* Basisform: Denne form foretrækkes i alkaliske opløsninger og har en anden farve.
2. Reaktion med syrer og alkalier:
* I sure opløsninger: Den høje koncentration af H+ ioner reagerer med indikatorens baseform og flytter ligevægten mod syreformen, som viser sin karakteristiske farve.
* I alkaliske opløsninger: Den høje koncentration af OH-ioner reagerer med indikatorens syreform og flytter ligevægten mod baseformen, som viser sin karakteristiske farve.
3. Almindelige indikatorer:
* Lakmuspapir: Bliver rød i sure opløsninger og blå i alkaliske opløsninger.
* Fenolphtalein: Farveløs i sure opløsninger og lyserød i alkaliske opløsninger.
* Methylorange: Rød i sure opløsninger og gul i alkaliske opløsninger.
* Universal indikator: En blanding af flere indikatorer, der skifter gennem en række farver, hvilket giver et mere præcist estimat af pH.
4. Sådan bruges indikatorer:
* Lakmuspapir: Dyp en strimmel lakmuspapir i opløsningen. Farveændringen angiver, om opløsningen er sur eller basisk.
* Væskeindikatorer: Tilsæt et par dråber af væskeindikatoren til opløsningen. Observer farveændringen.
* Universal indikator: Tilføj et par dråber universel indikator til opløsningen og sammenlign den resulterende farve med et diagram for at bestemme den omtrentlige pH.
Opsummering: Indikatorer virker ved at ændre farve baseret på pH i en opløsning. Dette giver os mulighed for nemt at identificere, om en opløsning er sur eller basisk, hvilket gør dem til værdifulde værktøjer i kemi og hverdagsliv.
 Varme artikler
Varme artikler
-
 Forskere tager et nyt kig på Michaelis-Menten-ligningenMagnus Kjærgaard (til venstre) og Mateusz Dyla udfordrer en af hjørnestenene i biokemi, Michaelis-Menten-ligningen, da de viser, at mange enzymer i signalveje er uafhængige af substratkoncentration,
Forskere tager et nyt kig på Michaelis-Menten-ligningenMagnus Kjærgaard (til venstre) og Mateusz Dyla udfordrer en af hjørnestenene i biokemi, Michaelis-Menten-ligningen, da de viser, at mange enzymer i signalveje er uafhængige af substratkoncentration, -
 Beregning af molær koncentration:En trin-for-trin guideTotojang/iStock/GettyImages At kunne beregne koncentrationen af en opløsning er en af de mest basale færdigheder, der kræves af en videnskabsmand. Uden at vide, hvor meget af et stof du arbejder med,
Beregning af molær koncentration:En trin-for-trin guideTotojang/iStock/GettyImages At kunne beregne koncentrationen af en opløsning er en af de mest basale færdigheder, der kræves af en videnskabsmand. Uden at vide, hvor meget af et stof du arbejder med, -
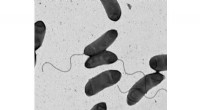 En usædvanlig form for antibiotikaresistens ved pandemisk koleraBilledet er et elektronmikrografi af bakterien Vibrio kolerae , det forårsagende middel til koleraen. Kredit:M. Stephen Trent, University of Georgia Kolera er en ødelæggende sygdom for millioner
En usædvanlig form for antibiotikaresistens ved pandemisk koleraBilledet er et elektronmikrografi af bakterien Vibrio kolerae , det forårsagende middel til koleraen. Kredit:M. Stephen Trent, University of Georgia Kolera er en ødelæggende sygdom for millioner -
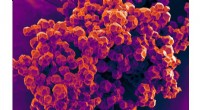 Maskinlæring forudsiger mekaniske egenskaber af porøse materialerKrystallinsk metal-organisk ramme. Kredit:David Fairen-Jimenez Maskinlæring kan bruges til at forudsige egenskaberne af en gruppe materialer, som, ifølge nogle, kunne være lige så vigtig for det 2
Maskinlæring forudsiger mekaniske egenskaber af porøse materialerKrystallinsk metal-organisk ramme. Kredit:David Fairen-Jimenez Maskinlæring kan bruges til at forudsige egenskaberne af en gruppe materialer, som, ifølge nogle, kunne være lige så vigtig for det 2
- Hvilken ejendom har betyder noget energi ikke?
- Hvilke symbiotiske forhold har en hvid aborre?
- NASA køber Moon dust for $1
- To caribiske fuglefangertræer opkaldt efter to kvinder med overset botaniske værker
- Jorden har brug for klimarealitetstjek, rumpioner advarer
- Fødevarer betyder noget:Sunde kostvaner øger den økonomiske og fysiske gennemførlighed af 1,5°C…


