Ammoniakopløsning i vand:Forståelse af NH3 + H2O-reaktionen
Her er en mere præcis fremstilling:
NH3 (aq) + H2O (l) ⇌ NH4+ (aq) + OH- (aq)
Forklaring:
* NH3 (vandig) :Ammoniak opløst i vand og danner en vandig opløsning.
* H2O (l) :Flydende vand.
* NH4+ (vandig) :Ammoniumion, en positivt ladet ion dannet, når ammoniak accepterer en proton (H+) fra vand.
* OH- (vandig) :Hydroxidion, en negativt ladet ion dannet, når vand mister en proton.
* ⇌ :Dobbeltpilen angiver, at reaktionen er reversibel. Det kan fortsætte i begge retninger, hvilket betyder, at ammonium- og hydroxidioner kan reagere og danne ammoniak og vand.
Nøglepunkter:
* Ligevægt: Reaktionen når en ligevægtstilstand, hvor hastighederne for de fremadrettede og omvendte reaktioner er ens.
* Grundlæggende løsning: Tilstedeværelsen af hydroxidioner (OH-) gør opløsningen basisk.
* Svag base: Ammoniak er en svag base, fordi den kun delvist ioniserer i vand, hvilket betyder, at den ikke donerer alle sine elektroner til at danne hydroxidioner.
Denne reaktion er vigtig, fordi den demonstrerer ammoniakens grundlæggende natur og dens evne til at acceptere protoner i vand. Det er også relevant for at forstå pH-værdien af opløsninger, der indeholder ammoniak.
 Varme artikler
Varme artikler
-
 Ionbindinger forklaret:Hvordan elektroner overføres til dannelse af stærke, ledende forbindelserSarapulSar38/iStock/GettyImages Hvad er en ionisk binding? I kemi opstår en ionbinding, når atomer med markant forskellige elektronegativiteter interagerer. Et atom, typisk et metal, donerer en elekt
Ionbindinger forklaret:Hvordan elektroner overføres til dannelse af stærke, ledende forbindelserSarapulSar38/iStock/GettyImages Hvad er en ionisk binding? I kemi opstår en ionbinding, når atomer med markant forskellige elektronegativiteter interagerer. Et atom, typisk et metal, donerer en elekt -
 Belysning af måden at skifte kemiske reaktionsvejeForskere brugte grøn laser til at modulere reaktiviteten af triazolinediones (TADer), kraftfulde kemiske koblingsmidler. Kredit:QUT Kunne fremstillingen af de integrerede kredsløb og chips til
Belysning af måden at skifte kemiske reaktionsvejeForskere brugte grøn laser til at modulere reaktiviteten af triazolinediones (TADer), kraftfulde kemiske koblingsmidler. Kredit:QUT Kunne fremstillingen af de integrerede kredsløb og chips til -
 Lavpris gelfilm kan plukke drikkevand fra ørkenluftenEn prototype enhed til at opfange vand fra luften ved hjælp af den nye film. Kredit:University of Texas i Austin Mere end en tredjedel af verdens befolkning bor i tørre områder, områder med betydel
Lavpris gelfilm kan plukke drikkevand fra ørkenluftenEn prototype enhed til at opfange vand fra luften ved hjælp af den nye film. Kredit:University of Texas i Austin Mere end en tredjedel af verdens befolkning bor i tørre områder, områder med betydel -
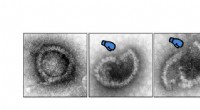 Et skridt på vejen mod bedre behandlinger mod viraEt elektronmikroskopbillede. Det viser, hvordan herpesvirus angribes af proteinet MxB. Kredit:Manutea Serrero &Beate Sodeik, Virology, Hannover Medical School, Tyskland. De fleste celler kan forsva
Et skridt på vejen mod bedre behandlinger mod viraEt elektronmikroskopbillede. Det viser, hvordan herpesvirus angribes af proteinet MxB. Kredit:Manutea Serrero &Beate Sodeik, Virology, Hannover Medical School, Tyskland. De fleste celler kan forsva


