CH3Li-bindingskarakter:Ionisk vs. kovalent - Forstå hybridnaturen
Her er hvorfor:
* Elektronegativitetsforskel: Elektronegativitetsforskellen mellem kulstof (2,55) og lithium (0,98) er relativt stor (1,57). Dette tyder på, at bindingen ville være polær med lithium, der bærer en delvis positiv ladning og kulstof en delvis negativ ladning.
* Lithiums metalliske natur: Lithium er et meget elektropositivt grundstof, hvilket betyder, at det let mister sin elektron for at danne en positiv ion (Li+).
* Struktur: Strukturen af CH3Li antyder en ionisk karakter. Det eksisterer som en polymer struktur, hvor lithiumioner er koordineret til kulstofatomer.
* Reaktivitet: CH3Li er en stærk base og nukleofil. Dens reaktivitet er i overensstemmelse med tilstedeværelsen af en meget polær eller ionbinding.
Bindingen mellem kulstof og lithium i CH3Li har dog også en kovalent karakter på grund af:
* Elektrondeling: Mens bindingen primært er ionisk, er der en vis grad af elektrondeling mellem kulstof og lithium.
* Forbindelsesstyrke: Bindingen er relativt stærk, hvilket typisk ikke ses ved rene ionbindinger.
Derfor beskrives CH3Li bedst som en ionforbindelse med en signifikant kovalent karakter.
 Varme artikler
Varme artikler
-
 Modificeret enzym kan øge anden generations ethanolproduktionVed at bruge et protein produceret af en svamp, der lever i Amazonas, Brasilianske forskere udviklede et molekyle, der er i stand til at øge glukosefrigivelsen fra biomasse til fermentering (sukkerrør
Modificeret enzym kan øge anden generations ethanolproduktionVed at bruge et protein produceret af en svamp, der lever i Amazonas, Brasilianske forskere udviklede et molekyle, der er i stand til at øge glukosefrigivelsen fra biomasse til fermentering (sukkerrør -
 Klart og effektivt lys uden sjældne metallerKredit:Mattias Lindh Moderne smartphone -skærme, samt mange andre effektive lyskilder, indeholde dyre og miljøproblematiske sjældne metaller. For en bæredygtig fremtid, ingeniører skal vende sig t
Klart og effektivt lys uden sjældne metallerKredit:Mattias Lindh Moderne smartphone -skærme, samt mange andre effektive lyskilder, indeholde dyre og miljøproblematiske sjældne metaller. For en bæredygtig fremtid, ingeniører skal vende sig t -
 Forskere udvikler ny teknik til produktion af plasmonics-enhederKredit:CC0 Public Domain Forskningslaboratorier udvikler konstant nye materialer, der forventes at udvise nye egenskaber, der er bundet til at revolutionere denne eller hin teknologi. Men det er i
Forskere udvikler ny teknik til produktion af plasmonics-enhederKredit:CC0 Public Domain Forskningslaboratorier udvikler konstant nye materialer, der forventes at udvise nye egenskaber, der er bundet til at revolutionere denne eller hin teknologi. Men det er i -
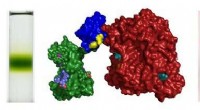 Team udvikler fotosyntetiske proteiner til udvidet solenergiomdannelseProteiner fra en grøn plante og en lilla bakterie låses sammen af et genetisk kodet grænseflade-domæne (blå/gul). Kredit:University of Bristol Et team af forskere, ledet af University of Bristol
Team udvikler fotosyntetiske proteiner til udvidet solenergiomdannelseProteiner fra en grøn plante og en lilla bakterie låses sammen af et genetisk kodet grænseflade-domæne (blå/gul). Kredit:University of Bristol Et team af forskere, ledet af University of Bristol
- Sådan virker solbriller
- Hvilke to genstande øges, når gravitationskraft falder?
- Mest primitive kænguru-forfader genopdaget efter 30 år i uklarhed
- Ethanol er et brændstof, der kan fremstilles af majs, hvor mange KJ varmeenergi frigøres, når der…
- Udforskning af konfliktens miljøpåvirkning
- Hvorfor blev Dagobah kaldt et system i stedet for planet?


