Aluminium og zinknitratreaktion:Forståelse af den kemiske proces
Aluminium er mere reaktivt end zink. Dette betyder, at aluminium vil fortrænge zink fra sin opløsning.
Reaktionen:
Reaktionen er en enkelt forskydningsreaktion:
* 2Al(s) + 3Zn(NO₃)₂(aq) → 2Al(NO₃)₃(aq) + 3Zn(s)
Forklaring:
* Aluminium (Al) vil reagere med zinknitrat (Zn(NO₃)₂) for at danne aluminiumnitrat (Al(NO₃)₃) og fast zink (Zn).
* Aluminiumsatomerne vil miste elektroner og blive til aluminiumioner (Al³⁺), som derefter vil kombineres med nitrationer (NO₃⁻) for at danne aluminiumnitrat.
* Zinkionerne (Zn²⁺) vil få elektroner og blive til zinkatomer, som vil udfældes fra opløsningen som fast zink.
Observationer:
* Du vil se et gråhvidt fast stof (zink) dannes på overfladen af aluminium.
* Opløsningen ville blive farveløs, efterhånden som zinknitratet forbruges.
* Aluminiumet kan blive udhulet, når det oxideres.
Vigtig bemærkning: Reaktionen vil forløbe langsomt ved stuetemperatur. Det kan fremskyndes ved at opvarme opløsningen eller øge overfladearealet af aluminium.
 Varme artikler
Varme artikler
-
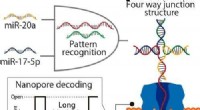 Nanopore-teknologi med DNA-beregning registrerer let mikroRNA-mønstre af lungekræftDNAer genkendte autonomt to mikroRNAer, miR-20a og miR-17-5p, og dannede en fire-vejs forbindelsesstruktur, der blev fanget i nanopore, viser lange blokeringsstrømme. Kredit:Figur tilpasset med tillad
Nanopore-teknologi med DNA-beregning registrerer let mikroRNA-mønstre af lungekræftDNAer genkendte autonomt to mikroRNAer, miR-20a og miR-17-5p, og dannede en fire-vejs forbindelsesstruktur, der blev fanget i nanopore, viser lange blokeringsstrømme. Kredit:Figur tilpasset med tillad -
 Et origami-inspireret medicinsk plaster til forsegling af indre skaderMIT-ingeniører har designpapirlignende medicinske tape (vist her), der kan foldes rundt om kirurgiske værktøjer og forvandles til bløde, stærke klæbemidler, når de presses mod væv. Kredit:Felice Frank
Et origami-inspireret medicinsk plaster til forsegling af indre skaderMIT-ingeniører har designpapirlignende medicinske tape (vist her), der kan foldes rundt om kirurgiske værktøjer og forvandles til bløde, stærke klæbemidler, når de presses mod væv. Kredit:Felice Frank -
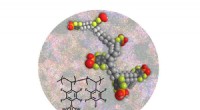 Banebrydende materiale gør vej til brintbrug til brændselsceller under varme, tørre forholdForskere har udviklet en protonleder til brændselsceller baseret på polystyrenphosphonsyrer, der opretholder høj protonisk ledningsevne ved høje temperaturer uden vand. Kredit:Los Alamos National Labo
Banebrydende materiale gør vej til brintbrug til brændselsceller under varme, tørre forholdForskere har udviklet en protonleder til brændselsceller baseret på polystyrenphosphonsyrer, der opretholder høj protonisk ledningsevne ved høje temperaturer uden vand. Kredit:Los Alamos National Labo -
 Præcise magneter 3-D printet af specielt rustfrit stålEmpa præcist magnetiseret:Jernspåner klæber til dette mini skakbræt med fire millimeter kantlængde. Den delvist magnetiske struktur blev fremstillet af en enkelt type stålkraft ved forskellige tempera
Præcise magneter 3-D printet af specielt rustfrit stålEmpa præcist magnetiseret:Jernspåner klæber til dette mini skakbræt med fire millimeter kantlængde. Den delvist magnetiske struktur blev fremstillet af en enkelt type stålkraft ved forskellige tempera
- Har blæksprutter, blæksprutter og krabber følelser?
- NASAs Terra-satellit fanger slutningen af Atlantic Tropical Depression 15
- Hvad sker der med den kinetiske energi af et stof, mens de gennemgår faseændring?
- Kompleks liv en milliard år tidligere end antaget?
- Nordvestlige borgerforskere blandt de mange, der hjælper med at spore solformørkelse over hele USA
- Hvordan vi vælger at stoppe skovrydning, vil påvirke fremtidige emissioner


