Syrer:definition, egenskaber og hvordan de frigiver hydrogenioner
Her er en opdeling:
* Syrer er kemiske forbindelser, der donerer protoner (H+) til andre stoffer.
* Brintioner (H+) er positivt ladede ioner, der dannes, når et brintatom mister sin elektron.
* Vandig opløsning refererer til en opløsning, hvor vand er opløsningsmidlet.
Når en syre opløses i vand, donerer den H+ ioner til vandmolekylerne. Dette resulterer i en stigning i koncentrationen af H+ ioner i opløsningen, hvilket gør opløsningen sur.
Eksempler på syrer:
* Saltsyre (HCl): Findes i mavesyre, brugt i industrielle processer.
* Svovlsyre (H2SO4): Anvendes i batterier, gødning og mange industrielle processer.
* Salpetersyre (HNO3): Anvendes til fremstilling af kunstgødning, sprængstoffer og plast.
* Eddikesyre (CH3COOH): Findes i eddike.
Styrken af en syre bestemmes af, hvor let den frigiver H+ ioner. Stærke syrer frigiver H+ ioner fuldstændigt, mens svage syrer kun frigiver en lille del af deres H+ ioner.
 Varme artikler
Varme artikler
-
 Fra at lave vin til at håndtere mineaffald, ler er vigtigt for mange industrierDe unikke egenskaber ved ler gør dem velegnede til en lang række anvendelser. Kredit:Shutterstock Opdagelsen og brugen af ler går tilbage til 30, 000 år siden, gør ler til et af de ældste materi
Fra at lave vin til at håndtere mineaffald, ler er vigtigt for mange industrierDe unikke egenskaber ved ler gør dem velegnede til en lang række anvendelser. Kredit:Shutterstock Opdagelsen og brugen af ler går tilbage til 30, 000 år siden, gør ler til et af de ældste materi -
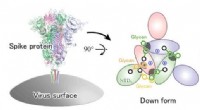 Glykaner er afgørende for COVID-19-infektionMolekylær mekanisme, der ligger til grund for den strukturelle ændring af SARS-CoV-2 spike-proteinet. Kredit:RIKEN En forskergruppe ved RIKEN Center for Computational Science (R-CCS) har fundet ud
Glykaner er afgørende for COVID-19-infektionMolekylær mekanisme, der ligger til grund for den strukturelle ændring af SARS-CoV-2 spike-proteinet. Kredit:RIKEN En forskergruppe ved RIKEN Center for Computational Science (R-CCS) har fundet ud -
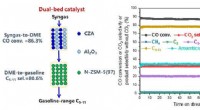 Dobbelts katalysator muliggør høj omdannelse af syngas til flydende carbonhydrider i benzininterva…Skematisk diagram for omdannelsen af syngas til flydende carbonhydrider i benzinområdet over en dobbeltbedskatalysator (CZA+Al2O3)/N-ZSM-5(97) og resultaterne af stabilitetstesten. Kredit:DICP B
Dobbelts katalysator muliggør høj omdannelse af syngas til flydende carbonhydrider i benzininterva…Skematisk diagram for omdannelsen af syngas til flydende carbonhydrider i benzinområdet over en dobbeltbedskatalysator (CZA+Al2O3)/N-ZSM-5(97) og resultaterne af stabilitetstesten. Kredit:DICP B -
 ChemMaps lader forskere navigere i det kemiske universChemMaps skærmbillede. Kredit:NC State University Forskere fra North Carolina State University har skabt en ny onlinetjeneste - ChemMaps - der giver brugerne mulighed for interaktivt at navigere i
ChemMaps lader forskere navigere i det kemiske universChemMaps skærmbillede. Kredit:NC State University Forskere fra North Carolina State University har skabt en ny onlinetjeneste - ChemMaps - der giver brugerne mulighed for interaktivt at navigere i
- Hvilken type binding findes i AlNi?
- Hvad er bryophytes?
- Hvilken type energi har en klemt kugle?
- Vedvarende spørgsmålstegn ved viden tager en vejafgift:Ny undersøgelse understøtter teorier om, …
- Nåletræskommunikation er kompleks og kan ændres af luftforurening
- Hvordan opnåede Archebacteria sin energi?


