Forståelse af kovalent bindingsdannelse:Elektronegativitetens rolle
* Elektronegativitet: Dette er et mål for et atoms evne til at tiltrække elektroner i en binding.
* Kovalente bindinger: Disse bindinger dannes, når atomer deler elektroner.
* Lignende elektronegativitet: Når atomer har lignende elektronegativiteter, har ingen af atomerne et stærkt nok træk til fuldstændigt at stjæle en elektron fra det andet. Det betyder, at de er mere tilbøjelige til at dele elektroner og danne en kovalent binding.
Eksempler:
* Ikke-metaller: Ikke-metaller har generelt relativt høj elektronegativitet. Når ikke-metaller binder med andre ikke-metaller, har de en tendens til at danne kovalente bindinger. For eksempel danner oxygen (O) og hydrogen (H) en kovalent binding i vand (H2O).
* Elementer i samme gruppe: Grundstoffer i samme gruppe på det periodiske system har ofte lignende elektronegativitet, hvilket gør dem mere tilbøjelige til at danne kovalente bindinger med hinanden. For eksempel danner kulstof (C) og silicium (Si) begge kovalente bindinger med andre ikke-metaller.
Vigtige overvejelser:
* Polære kovalente bindinger: Mens kovalente bindinger dannes ved at dele elektroner, kan delingen være ujævn. Hvis elektronegativitetsforskellen mellem to atomer er lille, men ikke nul, betragtes bindingen som polær kovalent.
* ioniske bindinger: Når elektronegativitetsforskellen mellem to atomer er stor, vil det ene atom fuldstændig stjæle en elektron fra det andet og danne en ionbinding.
Sammenfattende, jo tættere elektronegativitetsværdierne for to elementer er, jo mere sandsynligt er det, at de danner en kovalent binding.
 Varme artikler
Varme artikler
-
 Kemikere laver en måde at fjerne mikroplastik ved hjælp af okraOkra bruges som fortykningsmiddel i mange køkkener. Ekstrakter af okra og andre slimede planter, der almindeligvis anvendes til madlavning, kan hjælpe med at fjerne farlig mikroplastik fra spildeva
Kemikere laver en måde at fjerne mikroplastik ved hjælp af okraOkra bruges som fortykningsmiddel i mange køkkener. Ekstrakter af okra og andre slimede planter, der almindeligvis anvendes til madlavning, kan hjælpe med at fjerne farlig mikroplastik fra spildeva -
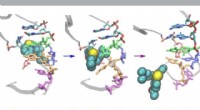 Supercomputere simulerer nye veje til potentiel behandling af RNA-virusStrukturelle ændringer i RNA under lægemiddelbinding/afbinding. Kredit:Lev Levintov, University of New Hampshire University of New Hampshire (UNH) forskere brugte for nylig Comet ved San Diego Sup
Supercomputere simulerer nye veje til potentiel behandling af RNA-virusStrukturelle ændringer i RNA under lægemiddelbinding/afbinding. Kredit:Lev Levintov, University of New Hampshire University of New Hampshire (UNH) forskere brugte for nylig Comet ved San Diego Sup -
 Hvor grøn er din vandtætte jakke?Kredit:University of Leeds I lyset af uforudsigelige vejrforhold, vandtætte jakker er blevet nøgleelementer i mange menneskers garderober. Men ny forskning fra University of Leeds tyder på, at br
Hvor grøn er din vandtætte jakke?Kredit:University of Leeds I lyset af uforudsigelige vejrforhold, vandtætte jakker er blevet nøgleelementer i mange menneskers garderober. Men ny forskning fra University of Leeds tyder på, at br -
 Computermodel til design af proteinsekvenser, der er optimeret til at binde til lægemiddelmålVed at bruge en computermodelleringstilgang, som de udviklede, MIT-biologer identificerede tre forskellige proteiner, der kan binde selektivt til hver af tre lignende mål, alle medlemmer af Bcl-2-fami
Computermodel til design af proteinsekvenser, der er optimeret til at binde til lægemiddelmålVed at bruge en computermodelleringstilgang, som de udviklede, MIT-biologer identificerede tre forskellige proteiner, der kan binde selektivt til hver af tre lignende mål, alle medlemmer af Bcl-2-fami
- Hvilke væv viser chloroplaster i overflod?
- Forbedring af siliciums egenskaber ved at erstatte brint med deuterium på overfladelaget
- 2015-2016 udløste El Nino sygdomsudbrud over hele kloden
- Er solvinden en del af Suns -atmosfæren?
- Elektronisk kamera i bordplade fanger ultrahurtig dynamik i sagen
- Hvad er de 5 egenskaber, der er fælles for alt liv på jorden?


