Forståelse af atomradius i kemiske bindinger:En omfattende vejledning
Her er hvorfor:
* Kovalent radius: Når to identiske atomer binder kovalent, deler de elektroner ligeligt. Afstanden mellem deres kerner betragtes som bindingslængden . Den kovalente radius er defineret som halvdelen af bindingslængden.
* Metallig radius: I metaller er atomer pakket tæt sammen i et gitter. Den metalliske radius er defineret som halvdelen af afstanden mellem to tilstødende kerner i det metalliske gitter.
Vigtig bemærkning: Atomradius er ikke en fast værdi. Det kan variere afhængigt af typen af binding, antallet af bindinger og elektronegativiteten af de involverede atomer.
 Varme artikler
Varme artikler
-
 Finjuster enhedens ydeevne med sværme af svømmecellerJ. Mark Meacham vender standardpraksis med at bruge mikrofluidisk værktøjer til videnskabelig opdagelse på hovedet ved at bruge en levende organisme til realtidsmåling og overvågning af akustisk mikro
Finjuster enhedens ydeevne med sværme af svømmecellerJ. Mark Meacham vender standardpraksis med at bruge mikrofluidisk værktøjer til videnskabelig opdagelse på hovedet ved at bruge en levende organisme til realtidsmåling og overvågning af akustisk mikro -
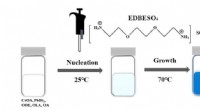 En ny strategi til at skabe blåt lys fra et lovende materialeSkemaet for syntesen af EDBESO4 behandlet CsPbBr3 NPLer. Kredit:Avancerede energimaterialer DOI:10.1002/aenm.202201605 Et forskningshold fra Florida State University har udviklet en ny måde at sk
En ny strategi til at skabe blåt lys fra et lovende materialeSkemaet for syntesen af EDBESO4 behandlet CsPbBr3 NPLer. Kredit:Avancerede energimaterialer DOI:10.1002/aenm.202201605 Et forskningshold fra Florida State University har udviklet en ny måde at sk -
 Sådan måles relativ fugtighed:En praktisk vejledning til studerende og vejrentusiasterAf Robin McDaniel | Opdateret 30. august 2022 Nøjagtig måling af luftens fugtindhold - kendt som relativ fugtighed (RH) - er afgørende for vejrrelaterede projekter, videnskabelige eksperimenter og hv
Sådan måles relativ fugtighed:En praktisk vejledning til studerende og vejrentusiasterAf Robin McDaniel | Opdateret 30. august 2022 Nøjagtig måling af luftens fugtindhold - kendt som relativ fugtighed (RH) - er afgørende for vejrrelaterede projekter, videnskabelige eksperimenter og hv -
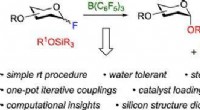 Syntetisering af sukker:Kemikere udvikler metode til at forenkle opbygning af kulhydraterKredit:ACS Kulhydrater er komplekse molekyler, svært at syntetisere i laboratoriet, men det er nyttigt at studere gavnlige sukkerarter, såsom dem, der findes i modermælk, eller gør det muligt for
Syntetisering af sukker:Kemikere udvikler metode til at forenkle opbygning af kulhydraterKredit:ACS Kulhydrater er komplekse molekyler, svært at syntetisere i laboratoriet, men det er nyttigt at studere gavnlige sukkerarter, såsom dem, der findes i modermælk, eller gør det muligt for
- Buten og brom:Forståelse af affarvningsreaktionen
- Hvilke par elementer er mest sandsynligt at danne en ionisk forbindelse Mg og F eller O Cl?
- Mod et bedre batteri:Forskere afslører kilde til nedbrydning i natriumbatterier
- Neutronstjerne smashup set for første gang, transformerer forståelsen af universet
- Hvorfor EU's skatteundersøgelse af Apple og andre vækker amerikansk vrede
- Livsenergiprocesser og fødevareproduktion?


