Brint- og iltreaktion i brændselsceller:En detaljeret forklaring
1. Brændstof (brint) input:
* Brintgas (H2) føres ind i brændselscellens anode, hvor den reagerer med en katalysator (typisk platin).
2. Oxidation ved anoden:
* Katalysatoren hjælper med at nedbryde brintmolekylerne til hydrogenioner (H+) og elektroner (e-):
* H2 → 2H+ + 2e-
3. Elektronstrøm:
* Elektronerne bevæger sig gennem et eksternt kredsløb og genererer elektricitet. Dette er brændselscellens energiudgang.
4. Iltindgang:
* Iltgas (O2) føres ind i brændselscellens katode.
5. Reduktion ved katoden:
* Iltmolekylerne reagerer med brintionerne (H+) og elektronerne (e-), der har rejst gennem det ydre kredsløb.
* Katalysatoren hjælper denne reaktion:
* O2 + 4H+ + 4e- → 2H2O
6. Vandudgang:
* Det endelige produkt af reaktionen er vand (H2O), som frigives som et biprodukt.
Samlet reaktion:
* Den overordnede kemiske reaktion i en brændselscelle kan opsummeres som:
* 2H2 + O2 → 2H2O
Nøgletræk ved brændselscelle-reaktioner:
* Ingen forbrænding: Reaktionen sker gennem en elektrokemisk proces, ikke ved afbrænding.
* Høj effektivitet: Brændselsceller omdanner kemisk energi til elektrisk energi med relativt høj effektivitet sammenlignet med forbrændingsmotorer.
* Ren energi: Det primære biprodukt er vand, hvilket gør brændselsceller til en ren energikilde.
* Kontinuerlig drift: Så længe der tilføres brint og ilt, kan brændselscellen fungere kontinuerligt.
Typer af brændselsceller:
Der findes forskellige typer brændselsceller, hver med sine egne driftsbetingelser og anvendelser. Almindelige typer omfatter:
* Proton Exchange Membrane (PEM) brændselsceller: Fungerer ved relativt lave temperaturer og bruges ofte i biler og bærbare enheder.
* Solid Oxide Fuel Cells (SOFC'er): Kører ved høje temperaturer og er velegnede til stationær elproduktion.
Brændselsceller er en lovende teknologi til at generere ren og effektiv energi. De har potentialet til at spille en væsentlig rolle i at reducere vores afhængighed af fossile brændstoffer og afbøde klimaændringer.
 Varme artikler
Varme artikler
-
 Brug af kemi til at låse op for forskellen mellem kold- og varmbrygget kaffeKredit:CC0 Public Domain Kold bryg kan være den hotteste trend inden for kaffefremstilling, men ikke meget er kendt om, hvordan denne proces ændrer drikkens kemiske egenskaber. Forskere rapportere
Brug af kemi til at låse op for forskellen mellem kold- og varmbrygget kaffeKredit:CC0 Public Domain Kold bryg kan være den hotteste trend inden for kaffefremstilling, men ikke meget er kendt om, hvordan denne proces ændrer drikkens kemiske egenskaber. Forskere rapportere -
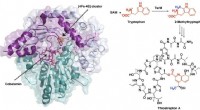 Syntese af potent antibiotikum følger en usædvanlig kemisk vejSyntesen af det potente antibiotikum thiostrepton bruger et radikalt SAM-protein TsrM, hvis krystalstruktur er vist til venstre, mens den er bundet til en jern-svovl-klynge og cobalamin. Nye billede
Syntese af potent antibiotikum følger en usædvanlig kemisk vejSyntesen af det potente antibiotikum thiostrepton bruger et radikalt SAM-protein TsrM, hvis krystalstruktur er vist til venstre, mens den er bundet til en jern-svovl-klynge og cobalamin. Nye billede -
 En fortælling om hyrder og spiralerKrigsskade med konsekvenser:efter Anden Verdenskrig, Giuseppe Torrettis marmorrelief Tilbedelse af hyrderne overlevede kun i fragmenter (brunlige sektioner), som er vist her i kombination med et sort
En fortælling om hyrder og spiralerKrigsskade med konsekvenser:efter Anden Verdenskrig, Giuseppe Torrettis marmorrelief Tilbedelse af hyrderne overlevede kun i fragmenter (brunlige sektioner), som er vist her i kombination med et sort -
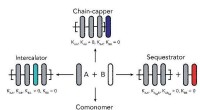 Styring af længden af supramolekylære polymererIllustration af, hvordan tilsætning af en anden supramolekylær polymer kan påvirke copolymerens længde. Kredit:Eindhoven University of Technology Systemer, der består af én supramolekylær polymer,
Styring af længden af supramolekylære polymererIllustration af, hvordan tilsætning af en anden supramolekylær polymer kan påvirke copolymerens længde. Kredit:Eindhoven University of Technology Systemer, der består af én supramolekylær polymer,
- Hvad er en mulig forklaring på formationer af galakser?
- Forskning har til formål automatisk at besvare brugerspørgsmål om online privatlivspolitikker
- Hvordan påvirker naturkræfter Jorden?
- Første bevis på kvantecomputerfordel
- Hvad er cellen fra en organisme, som en virus afhænger af?
- Hvordan ville densitet påvirke termisk energi?


