Hvorfor NaCl koger ved en meget højere temperatur end C4H10 - Forklaret
* Ionisk vs. kovalent binding: NaCl er en ionisk forbindelse, hvilket betyder, at den danner en krystalgitterstruktur, der holdes sammen af stærke elektrostatiske kræfter mellem positivt ladede natriumioner (Na⁺) og negativt ladede chloridioner (Cl⁻). C₄H₁₀ (butan) er en kovalent forbindelse med molekyler holdt sammen af relativt svage Van der Waals-kræfter.
* Styrken af intermolekylære kræfter: De elektrostatiske kræfter i ioniske forbindelser er betydeligt stærkere end Van der Waals-kræfterne i kovalente forbindelser. Denne forskel i styrken af intermolekylære kræfter er den primære årsag til den enorme kogepunktsforskel.
Sådan oversættes det til kogepunkt:
* NaCl: For at bryde de stærke ionbindinger i NaCl og få det til at koge, skal du tilføre en enorm mængde energi, hvilket resulterer i et meget højt kogepunkt (over 1400°C).
* C₄H₁₀: De svage Van der Waals-kræfter i butan overvindes let med relativt lidt energi, hvilket fører til et meget lavere kogepunkt (-0,5°C).
Opsummering:
* NaCl: Stærke ionbindinger =høje smelte- og kogepunkter
* C₄H₁₀: Svage Van der Waals-kræfter =lave smelte- og kogepunkter
 Varme artikler
Varme artikler
-
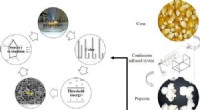 Store, velsmagende popcornkerner med infrarød tilberedningKredit:ACS Food Science &Technology (2022). DOI:10.1021/acsfoodscitech.2c00188 Ingen filmoplevelse er komplet uden popcorn, uanset om det er almindeligt, smørret eller overtrukket med sødt eller kr
Store, velsmagende popcornkerner med infrarød tilberedningKredit:ACS Food Science &Technology (2022). DOI:10.1021/acsfoodscitech.2c00188 Ingen filmoplevelse er komplet uden popcorn, uanset om det er almindeligt, smørret eller overtrukket med sødt eller kr -
 Forskere udvider retsmedicinsk metode til at identificere mennesker, der bruger proteiner fra knogle…LLNL -forskere Katelyn Mason og Deon Anex forbereder sig på at pulverisere kriminaltekniske prøver før demineralisering og ekstraktion af proteiner for at finde identitetsmarkører. Ud over tidligere a
Forskere udvider retsmedicinsk metode til at identificere mennesker, der bruger proteiner fra knogle…LLNL -forskere Katelyn Mason og Deon Anex forbereder sig på at pulverisere kriminaltekniske prøver før demineralisering og ekstraktion af proteiner for at finde identitetsmarkører. Ud over tidligere a -
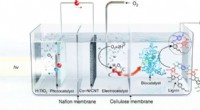 Nyt biokatalytisk system gør affaldsbiomasse til værdiskabende kemikalierSkematisk illustration af den tre-rums foto-elektro-biokemiske reaktor. Kredit:UNIST Et forskerhold, i fællesskab ledet af professor Ji Wook Jang, Professor Yong Hwan Kim, og professor Sang Hoon J
Nyt biokatalytisk system gør affaldsbiomasse til værdiskabende kemikalierSkematisk illustration af den tre-rums foto-elektro-biokemiske reaktor. Kredit:UNIST Et forskerhold, i fællesskab ledet af professor Ji Wook Jang, Professor Yong Hwan Kim, og professor Sang Hoon J -
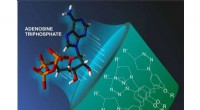 Fælder for energikildemolekyler i cellerKredit:Natalia Deryugina Et team af forskere, inklusive en RUDN-kemiker, har syntetiseret nye molekyler, der tilhører klassen af calixarener, skållignende hule strukturer. Disse stoffer ser ud t
Fælder for energikildemolekyler i cellerKredit:Natalia Deryugina Et team af forskere, inklusive en RUDN-kemiker, har syntetiseret nye molekyler, der tilhører klassen af calixarener, skållignende hule strukturer. Disse stoffer ser ud t
- Hvorfor citeres kvinder sjældnere end mænd?
- Sådan virker alkoholtermometre:Design, funktion og praktisk brug
- Hvilke redskaber bruges til at lokalisere en tornado?
- Hvor og hvordan blev energien opbevaret, før den blev overført til pumpning af dæk?
- Hvad er de to metaller, der udgør kerne?
- Celler nedbryder mad i en kemisk reaktion, der frigiver energi Hvilken proces er dette?


