Redox Titrering:Forstå principperne og anvendelserne
Redox Titrering:En dans af elektroner
Redox-titrering, ligesom dets syre-base-modstykke, er en kraftfuld analytisk teknik, der bruges til at bestemme koncentrationen af en ukendt opløsning. Men i stedet for at fokusere på protonoverførsel, kredser det om overførsel af elektroner mellem analytten (ukendt opløsning) og en titrant (opløsning med kendt koncentration).
Her er opdelingen:
1. Princippet:
- Redox-reaktion: Hjertet i redoxtitreringen ligger i en redoxreaktion mellem analytten og titranten. Denne reaktion involverer overførsel af elektroner, hvor den ene art oxideres (taber elektroner) og den anden reduceres (får elektroner).
- Ækvivalenspunkt: Titreringen fortsætter, indtil ækvivalenspunktet er nået. Dette er det punkt, hvor analytten og titranten har reageret fuldstændigt, hvilket betyder, at alt oxidationsmidlet er blevet reduceret, og alt reduktionsmidlet er blevet oxideret.
- Indikator: For visuelt at identificere ækvivalenspunktet bruges en redoxindikator ofte. Denne indikator ændrer farve ved et specifikt potentiale, hvilket signalerer færdiggørelsen af reaktionen.
2. Sådan fungerer det:
- Titrant: Titranten indeholder en kendt koncentration af et oxidations- eller reduktionsmiddel.
- Analyt: Den ukendte opløsning indeholder den analyt, du ønsker at bestemme koncentrationen af.
- Reaktion: Når titranten tilsættes dråbevis til analytten, finder en redoxreaktion sted.
- Ækvivalenspunkt: Ækvivalenspunktet nås, når den støkiometriske mængde titrant er blevet tilsat for fuldstændigt at reagere med analytten.
- Beregninger: Volumenet af titrant anvendt ved ækvivalenspunktet bruges derefter til at beregne koncentrationen af analytten ved at anvende den kendte koncentration af titranten og reaktionens støkiometri.
3. Applikationer:
Redox-titrering er meget udbredt inden for forskellige områder, herunder:
- Miljøkemi: Bestemmelse af koncentrationen af forurenende stoffer som tungmetaller og oxidanter.
- Fødevarekemi: Analyse af C-vitaminindholdet i frugt og grøntsager.
- Farmaceutisk industri: Bestemmelse af renheden og styrken af lægemidler og medicin.
- Industrikemi: Måling af koncentrationen af metaller, halogenider og andre stoffer i forskellige industrielle processer.
4. Eksempler:
- Bestemmelse af koncentrationen af jern(II)-ioner under anvendelse af kaliumpermanganat som titrant. Permanganationer (MnO4-) fungerer som et oxidationsmiddel, der omdanner jern(II)-ioner til jern(III)-ioner. Slutpunktet er angivet med den vedvarende lyserøde farve af permanganationerne.
- Bestemmelse af koncentrationen af jod ved hjælp af natriumthiosulfat som titrant. Jod virker som et oxidationsmiddel, og natriumthiosulfat virker som et reduktionsmiddel. Slutpunktet er angivet ved forsvinden af den brune farve af jod.
I bund og grund er redoxtitrering et effektivt værktøj til at analysere koncentrationen af stoffer ved at udnytte kraften i elektronoverførselsreaktioner.
Sidste artikelNaCl &AgNO3-reaktion:Forståelse af udfældningsprocessen
Næste artikelOpløselighed:Forstå hvordan stoffer opløses
 Varme artikler
Varme artikler
-
 Hold din salat frisk:Det enkle papirhåndklædetrick, der stopper brunhedenMichael Siluk/Getty Images Vi modtager muligvis en kommission på køb foretaget fra links. Intet er mere skuffende end at åbne en pose salat, der har brugt et par dage i køleskabet, kun for at finde
Hold din salat frisk:Det enkle papirhåndklædetrick, der stopper brunhedenMichael Siluk/Getty Images Vi modtager muligvis en kommission på køb foretaget fra links. Intet er mere skuffende end at åbne en pose salat, der har brugt et par dage i køleskabet, kun for at finde -
 At se nærmere på genetiske skift i kræftEn krystalstruktur af en del af menneskelig DPF2, et protein, der styrer en genetisk switch, der fortæller blodstamceller, hvornår de skal blive røde og hvide blodlegemer. Orange og gule områder illus
At se nærmere på genetiske skift i kræftEn krystalstruktur af en del af menneskelig DPF2, et protein, der styrer en genetisk switch, der fortæller blodstamceller, hvornår de skal blive røde og hvide blodlegemer. Orange og gule områder illus -
 Forskere tilbyder virksomheder en ny kemi for grønnere polyurethanEn banebrydende formel for vedvarende energi-NREL-forsker Tao Dong (højre) og tidligere praktikant Stephanie Federle (til venstre) undersøger biobaseret, ikke -toksisk polyurethanharpiks, et lovende a
Forskere tilbyder virksomheder en ny kemi for grønnere polyurethanEn banebrydende formel for vedvarende energi-NREL-forsker Tao Dong (højre) og tidligere praktikant Stephanie Federle (til venstre) undersøger biobaseret, ikke -toksisk polyurethanharpiks, et lovende a -
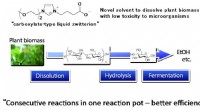 Nyt opløsningsmiddel bidrager til næste generations biobrændstofproduktion fra biomasseEfter opløsning af plantebiomasse med det nye opløsningsmiddel, flydende zwitterion af carboxylattypen, hydrolyse og fermentering blev udført fortløbende i en reaktionsbeholder til omdannelse til etha
Nyt opløsningsmiddel bidrager til næste generations biobrændstofproduktion fra biomasseEfter opløsning af plantebiomasse med det nye opløsningsmiddel, flydende zwitterion af carboxylattypen, hydrolyse og fermentering blev udført fortløbende i en reaktionsbeholder til omdannelse til etha
- Ny metode giver forskere mulighed for hurtigt at se individuelle viruspartikler
- Hvordan ændrer tiden for planeten til kredsløb solen med sin afstand fra solen?
- Harley-Davidson:ingen amerikansk salg ramt af offshoring dustup
- Forståelse af 9-kulstofkulhydrater:formler og strukturer
- Hvorfor præsenterer lysosomer kun en dyreceller?
- Bakterier med syntetisk genkredsløb samler sig selv for at bygge arbejdsenhed med guldnanopartikler


