Beregning af frysepunktsdepression:Benzen i kloroform
1. Forstå konceptet
* Frysepunktsdepression: Når et ikke-flygtigt opløst stof (som benzen) opløses i et opløsningsmiddel (som chloroform), falder opløsningens frysepunkt sammenlignet med det rene opløsningsmiddel.
* Frysepunktsdepressionsligning: ΔTf =Kf *m
* ΔTf =Ændring i frysepunktet
* Kf =Kryoskopisk konstant for opløsningsmidlet (for chloroform, Kf =4,68 °C/m)
* m =Molalitet af opløsningen (mol opløst stof pr. kg opløsningsmiddel)
2. Beregn molalitet (m)
* Muldvarp benzen:
* Molær masse af benzen (C6 H6 ) =78,11 g/mol
* Mol benzen =(2,50 g) / (78,11 g/mol) =0,0320 mol
* Masse kloroform i kg:
* 120 g =0,120 kg
* Moralitet:
* m =(0,0320 mol) / (0,120 kg) =0,267 mol/kg
3. Beregn ændringen i frysepunktet (ΔTf )
* ΔTf =(4,68 °C/m) * (0,267 mol/kg) =1,25 °C
4. Bestem frysepunktet for opløsningen
* Frysepunkt for ren kloroform: -63,5 °C
* Løsningens frysepunkt: -63,5 °C - 1,25 °C =-64,75 °C
Derfor er frysepunktet for opløsningen indeholdende 2,50 g benzen i 120 g chloroform -64,75 °C.
Sidste artikelBeregning af frysepunktsdepression:NiSO4-løsning
Næste artikelNøjagtig måling af syre med pH-strimler:en trin-for-trin guide
 Varme artikler
Varme artikler
-
 Et hjertesundt protein fra klid af kornafgrøderKredit:CC0 Public Domain Rævehale hirse er et etårigt græs, der dyrkes bredt som en kornafgrøde i dele af Indien, Kina og Sydøstasien. Maling af kornet fjerner det hårde ydre lag, eller klid, fra
Et hjertesundt protein fra klid af kornafgrøderKredit:CC0 Public Domain Rævehale hirse er et etårigt græs, der dyrkes bredt som en kornafgrøde i dele af Indien, Kina og Sydøstasien. Maling af kornet fjerner det hårde ydre lag, eller klid, fra -
 Ny forskning forklarer, hvorfor nogle molekyler har uregelmæssige formerKredit:Vanderbilt University Der er altid en grund til, hvordan molekyler dannes, og hvordan de er formet. Når først forskere forstår bindingerne i molekyler, de finder ud af måder at bruge de mat
Ny forskning forklarer, hvorfor nogle molekyler har uregelmæssige formerKredit:Vanderbilt University Der er altid en grund til, hvordan molekyler dannes, og hvordan de er formet. Når først forskere forstår bindingerne i molekyler, de finder ud af måder at bruge de mat -
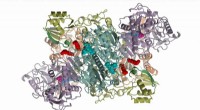 Molekylært maskineri, der fremstiller potent antibiotika, afsløret efter årtiers forskning3D-strukturen af McbBCD, et enzym (protein), der laver det potente antibiotikum mikrocin B17 fra et mindre protein kendt som et peptid, som afsløret ved røntgenkrystallografi. De røde kugler viser k
Molekylært maskineri, der fremstiller potent antibiotika, afsløret efter årtiers forskning3D-strukturen af McbBCD, et enzym (protein), der laver det potente antibiotikum mikrocin B17 fra et mindre protein kendt som et peptid, som afsløret ved røntgenkrystallografi. De røde kugler viser k -
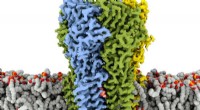 Undersøg detaljer om, hvordan generel bedøvelse og benzoer virker på receptorer i hjernenEn tredimensionel struktur af typen A GABA-receptor bundet med GABA og propofol indlejret i en cellemembran. Propofol er det mest almindeligt anvendte intravenøse bedøvelsesmiddel og virker gennem rec
Undersøg detaljer om, hvordan generel bedøvelse og benzoer virker på receptorer i hjernenEn tredimensionel struktur af typen A GABA-receptor bundet med GABA og propofol indlejret i en cellemembran. Propofol er det mest almindeligt anvendte intravenøse bedøvelsesmiddel og virker gennem rec
- En almindelig lipid til energilagring er?
- Augmented reality 'sandkasse' viser, hvordan tyngdekraften fungerer
- Hvor mange centre er der i NASA?
- Forskere afslører, hvordan en lidet kendt amøbe opslugte bakterien for at blive fotosyntetisk
- Mayaen. Ophørte civilisationen på grund af klimaændringer?
- Hvad er den hastighed, hvormed hastighedsændring kaldes?


