Elektrolyse af natriumchlorid:Forståelse af hydrogen- og natriumindsamling
Grundlæggende om elektrolyse
* Elektrolyse: Processen med at bruge en elektrisk strøm til at drive en ikke-spontan kemisk reaktion.
* Katode: Den negativt ladede elektrode, hvor der sker reduktion (forstærkning af elektroner).
* Anode: Den positivt ladede elektrode, hvor der sker oxidation (tab af elektroner).
Reaktionerne
Under elektrolysen af NaCl opstår følgende reaktioner:
* Ved katoden (reduktion):
* 2H2O(l) + 2e⁻ → H2(g) + 2OH⁻(vandig) Dette er reduktionen af vand til dannelse af brintgas.
* Ved anoden (oxidation):
* 2Cl⁻(vandig) → Cl2(g) + 2e⁻ Dette er oxidation af chloridioner til dannelse af klorgas.
Hvorfor hydrogen, ikke natrium?
1. Elektrokemisk serie: Den elektrokemiske serie (eller aktivitetsserie) lister metaller i rækkefølge efter deres reaktivitet. Natrium er et meget reaktivt metal, hvilket betyder, at det let taber elektroner. Brint er mindre reaktivt.
* Natrium er mere tilbøjelige til at blive oxideret (taber elektroner) ved anoden, IKKE katoden.
* Det er mere sandsynligt, at hydrogen reduceres (forstærker elektroner) ved katoden.
2. Overpotentiale: Overpotentialet er den ekstra spænding, der skal til for at overvinde energibarrieren, for at en reaktion kan opstå. Overpotentialet for reduktion af natriumioner er væsentligt højere end for reduktion af vand. Dette gør reduktionen af vand til brint til den mere gunstige proces ved katoden.
I oversigt
* Elektrokemisk reaktivitet: Brint er mindre reaktivt end natrium, hvilket gør det mere sandsynligt, at det reduceres ved katoden.
* Overpotentiale: Overpotentialet for hydrogenreduktion er lavere, hvilket favoriserer dannelsen af det frem for natrium.
Bemærk: Hvis du skulle bruge en kviksølvkatode, ville overpotentialet for natriumreduktion blive sænket, og du kan få natriummetal produceret ved katoden. Dette er dog en meget farlig proces.
Sidste artikelMg²⁺:Lewis-syreegenskaber og reaktivitet forklaret
Næste artikelForstå det grundlæggende ved calciumoxidopløsninger
 Varme artikler
Varme artikler
-
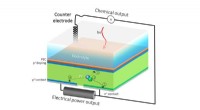 En solcelle, der gør dobbelt pligt til vedvarende energiHPEV -cellens ekstra stikkontakt gør det muligt at opdele strømmen i to, så en del af strømmen bidrager til produktion af solbrændstoffer, og resten kan udvindes som elektrisk strøm. Kredit:Berkeley L
En solcelle, der gør dobbelt pligt til vedvarende energiHPEV -cellens ekstra stikkontakt gør det muligt at opdele strømmen i to, så en del af strømmen bidrager til produktion af solbrændstoffer, og resten kan udvindes som elektrisk strøm. Kredit:Berkeley L -
 Glycerolphosphat tjener som en terminator for glykanforlængelse ved maligne kræftformerØget ekspression af PCYT2, som syntetiserer CDP-Gro i cancer, forbedrer GroP-modifikation og forringer matriglycandannelse. Dette fænomen gør det muligt for cancerceller at forlade begrænsningerne af
Glycerolphosphat tjener som en terminator for glykanforlængelse ved maligne kræftformerØget ekspression af PCYT2, som syntetiserer CDP-Gro i cancer, forbedrer GroP-modifikation og forringer matriglycandannelse. Dette fænomen gør det muligt for cancerceller at forlade begrænsningerne af -
 Bæredygtige biosyntetiske transparente film udviklet til plasterstatningKredit:Unsplash/CC0 Public Domain I dag er der ingen mulighed for at komme væk fra plastik. Vi producerer over 300 millioner tons plast hvert år, hvoraf over 40% fremstilles til film til emballeri
Bæredygtige biosyntetiske transparente film udviklet til plasterstatningKredit:Unsplash/CC0 Public Domain I dag er der ingen mulighed for at komme væk fra plastik. Vi producerer over 300 millioner tons plast hvert år, hvoraf over 40% fremstilles til film til emballeri -
 Binding af metan med metal:Et nyt håb om at genbruge det potente fossile brændstofi stand til at blive transporteret, bliver metan et biprodukt, der brændes (eller blusses) ved kilden, hvilket er både spild og uhyre forurenende. Kredit:Shutterstock UNSW kemikere har konstrueret
Binding af metan med metal:Et nyt håb om at genbruge det potente fossile brændstofi stand til at blive transporteret, bliver metan et biprodukt, der brændes (eller blusses) ved kilden, hvilket er både spild og uhyre forurenende. Kredit:Shutterstock UNSW kemikere har konstrueret
- Hvis man antager, at det vil regne, når himlen er overskyet og mørk et eksempel på a(n)?
- Byer verden over tog plads til biler og gav den til folk under pandemien. Vil det holde fast?
- Mendels lov om uafhængigt sortiment:definition, forklaring og praktiske eksempler
- Studiet af Perry Mason forsøger at bekæmpe uskyld træthed
- I hvilke afkom vises en dominerende egenskab?
- Gennembrud i nonoxidativ kobling af metan:Direkte omdannelse til propylen ved lav temperatur


