Kemiske bindinger og energiudveksling:Brydning og dannelse
Energiinput (Breaking Bonds):
* Endotermiske reaktioner: Reaktioner, der absorberer energi fra deres omgivelser.
* Båndbrud: Når energi tilføres et system, kan den bruges til at overvinde de kræfter, der holder atomer sammen i et molekyle. Denne energiinput svækker bindingerne, hvilket i sidste ende får dem til at bryde.
* Eksempler:
* Smeltende is:Energiinput bryder hydrogenbindingerne, der holder vandmolekyler sammen i fast tilstand.
* Fotosyntese:Sollys giver energi til at nedbryde kuldioxid og vandmolekyler, hvilket gør det muligt for planter at skabe sukker.
Energioutput (dannelse af obligationer):
* Eksotermiske reaktioner: Reaktioner, der frigiver energi til deres omgivelser.
* Obligationsdannelse: Når der dannes nye bindinger mellem atomer, frigives energi. Dette skyldes, at atomerne bliver mere stabile ved at dele elektroner og frigive den overskydende energi som varme eller lys.
* Eksempler:
* Afbrænding af træ:Brydning af bindinger i træet frigiver energi, som afgives som varme og lys.
* Forbrænding:Afbrænding af brændstoffer som benzin involverer at bryde eksisterende bindinger og danne nye bindinger i produkterne, frigive energi som varme og lys.
Nøglepunkter:
* Energi bevares: Den samlede energi i et system forbliver konstant. Energi bliver ikke skabt eller ødelagt, bare overført eller transformeret.
* Forbindelsesstyrke: Forskellige bindinger har forskellige styrker. Stærkere bindinger kræver mere energi for at bryde, og deres dannelse frigiver mere energi.
* Aktiveringsenergi: Selv eksoterme reaktioner kræver en indledende tilførsel af energi (aktiveringsenergi) for at starte bindingsbrudsprocessen.
I bund og grund er brydning og dannelse af kemiske bindinger grundlæggende for energiudveksling i kemiske reaktioner. Energi absorberes for at bryde bindinger, og energi frigives, når bindinger dannes.
 Varme artikler
Varme artikler
-
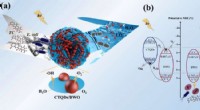 Forskere udvikler Z-skema katalysator for forurenende stoffer i vandSkematisk illustration af fotokatalytisk mekanisme. Kredit:YANG Pengqi I de seneste år, den hurtige industrialisering har forårsaget stadig mere alvorlig miljøforurening. Antibiotika og mikrobiolo
Forskere udvikler Z-skema katalysator for forurenende stoffer i vandSkematisk illustration af fotokatalytisk mekanisme. Kredit:YANG Pengqi I de seneste år, den hurtige industrialisering har forårsaget stadig mere alvorlig miljøforurening. Antibiotika og mikrobiolo -
 Du smører tro det:Pålæg med lavt kalorieindhold, hovedsagelig lavet af vandDoktorgradskandidat Michelle Lee, forgrunden, og postdoc-forsker Chen Tan arbejder i laboratoriet i Alireza Abbaspourrad for at udvikle et smøragtigt smørepålæg, der hovedsageligt består af vand. Kred
Du smører tro det:Pålæg med lavt kalorieindhold, hovedsagelig lavet af vandDoktorgradskandidat Michelle Lee, forgrunden, og postdoc-forsker Chen Tan arbejder i laboratoriet i Alireza Abbaspourrad for at udvikle et smøragtigt smørepålæg, der hovedsageligt består af vand. Kred -
 Hvor grøn er din vandtætte jakke?Kredit:University of Leeds I lyset af uforudsigelige vejrforhold, vandtætte jakker er blevet nøgleelementer i mange menneskers garderober. Men ny forskning fra University of Leeds tyder på, at br
Hvor grøn er din vandtætte jakke?Kredit:University of Leeds I lyset af uforudsigelige vejrforhold, vandtætte jakker er blevet nøgleelementer i mange menneskers garderober. Men ny forskning fra University of Leeds tyder på, at br -
 Ny metode muliggør effektiv prøveforberedelse til enkeltcellet proteomikKredit:Kumamoto University Proteinerne, der udgør vores celler, rummer en hel verden af information, som, når de er låst op, kan give os indsigt i oprindelsen af mange væsentlige biologiske fæn
Ny metode muliggør effektiv prøveforberedelse til enkeltcellet proteomikKredit:Kumamoto University Proteinerne, der udgør vores celler, rummer en hel verden af information, som, når de er låst op, kan give os indsigt i oprindelsen af mange væsentlige biologiske fæn
- Er der en ikke-levende ting, der reagerer på miljøet?
- Stenskibe viser tegn på maritimt netværk i Østersøområdet for 3.000 år siden
- Hvad er et værktøj, der tillader undersøgelse af mange gener og deres interaktioner på én gang?…
- Hvis et vakuum har hyppighed på 1.01000000000000000000, hvad er bølgelængden?
- Hvad findes der i DNA'et?
- Hvad er vinklen mellem Ray, der slår en overflade og vinkelret på ved kontaktpunktet?


