Ioniske bindinger:styrke, dannelse og egenskaber - en omfattende forklaring
* Elektrostatisk tiltrækning: Ionbindinger dannes af den elektrostatiske tiltrækning mellem modsat ladede ioner. Denne tiltrækning er meget stærk, især når ionerne har høje ladninger.
* Gitterstruktur: Ioniske forbindelser danner en krystalgitterstruktur, hvor ioner er arrangeret i et regelmæssigt, gentaget mønster. Denne struktur maksimerer de elektrostatiske tiltrækninger mellem ioner, hvilket gør bindingen endnu stærkere.
* Høje smelte- og kogepunkter: De stærke elektrostatiske kræfter i ionbindinger kræver meget energi at overvinde. Dette er grunden til, at ioniske forbindelser typisk har høje smelte- og kogepunkter.
* Opløselighed i polære opløsningsmidler: Ioniske forbindelser har en tendens til at opløses i polære opløsningsmidler (som vand), fordi de polære opløsningsmiddelmolekyler kan omgive og adskille ionerne og bryde ionbindingerne.
Hvorfor de kan virke "svage" i nogle sammenhænge:
* Opløselighed: Mens ionbindinger er stærke, kan de brydes af polære opløsningsmidler. Dette er grunden til, at ioniske forbindelser kan opløses i vand, hvilket får dem til at fremstå "svage" i denne sammenhæng.
* Hydrering: Når ioniske forbindelser opløses i vand, bliver ionerne omgivet af vandmolekyler (hydrering). Dette kan i nogen grad svække den elektrostatiske tiltrækning mellem ionerne.
Opsummering: Ionbindinger er iboende stærke på grund af den kraftige elektrostatiske tiltrækning mellem ioner. De kan dog blive påvirket af faktorer som opløselighed og hydrering, hvilket kan få dem til at virke "svage" i visse situationer.
Sidste artikelHvad er den flydende fase af vand?
Næste artikelCarbonatoxidationsnummer:En trin-for-trin forklaring (+4)
 Varme artikler
Varme artikler
-
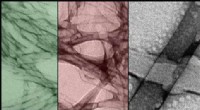 Formskiftende materialer:Brug af lys til at omarrangere makroskopiske strukturerTEM-billeder af selvsamlende nanostrukturer og deres rekombinationer, i falske farver. Kredit:Okinawa Institute of Science and Technology Graduate University - OIST OIST-forskere skaber selvsamlen
Formskiftende materialer:Brug af lys til at omarrangere makroskopiske strukturerTEM-billeder af selvsamlende nanostrukturer og deres rekombinationer, i falske farver. Kredit:Okinawa Institute of Science and Technology Graduate University - OIST OIST-forskere skaber selvsamlen -
 Mastering Buffer Solutions:Trin-for-trin guide til stabile pH-miljøerAf Carla Boulianne Opdateret 24. marts 2022 Bufferopløsninger modstår ændringer i pH, fordi de indeholder svage syre-base-konjugater, der neutraliserer H+ og OH-ioner. Bufferopløsninger består af s
Mastering Buffer Solutions:Trin-for-trin guide til stabile pH-miljøerAf Carla Boulianne Opdateret 24. marts 2022 Bufferopløsninger modstår ændringer i pH, fordi de indeholder svage syre-base-konjugater, der neutraliserer H+ og OH-ioner. Bufferopløsninger består af s -
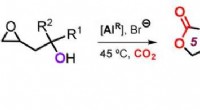 Kaskader med kuldioxidKredit: Angewandte Chemie Kuldioxid (CO 2 ) er ikke bare en uønsket drivhusgas, det er også en interessant kilde til råvarer, der er værdifulde og kan genbruges bæredygtigt. I journalen Angewa
Kaskader med kuldioxidKredit: Angewandte Chemie Kuldioxid (CO 2 ) er ikke bare en uønsket drivhusgas, det er også en interessant kilde til råvarer, der er værdifulde og kan genbruges bæredygtigt. I journalen Angewa -
 Nyt værktøj analyserer sygdom og lægemiddeleffekter med enestående nøjagtighed og konsistensSammenlignet med OpenMS og branchestandarden MaxQuant, IonStar sænkede mængden af manglende data i testresultater fra 17 procent til 0,1 procent. Det hvide område angiver manglende data. Kredit:Jun
Nyt værktøj analyserer sygdom og lægemiddeleffekter med enestående nøjagtighed og konsistensSammenlignet med OpenMS og branchestandarden MaxQuant, IonStar sænkede mængden af manglende data i testresultater fra 17 procent til 0,1 procent. Det hvide område angiver manglende data. Kredit:Jun
- Hvad er to typer opløsningsmidler?
- Kan der høres et vækkeur på månen?
- Hvilken organisk forbindelse produceres, når tre fedtsyremolekylebinding til et glycerolmolekyle?
- Blåt farvestof fra rødbeder:Kemikere udtænker en ny pigmentmulighed
- High School Investigatory Projects
- Video:Hvilken af disse svampe kan dræbe dig?


