Kulbrintestater:Forståelse af gas-, væske- og faststofegenskaber
* Molekylvægt: Større kulbrinter har flere atomer og en større molekylvægt. Dette fører til stærkere London-spredningskræfter, de midlertidige attraktioner mellem molekyler. Stærkere attraktioner kræver mere energi at overvinde, hvilket oversættes til højere kogepunkter.
* Forgreninger: Forgrenede kulbrinter har lavere kogepunkter end deres ligekædede modstykker. Dette skyldes, at forgrening reducerer molekylets overfladeareal, hvilket svækker London-spredningskræfterne mellem molekyler.
Her er en opdeling:
* Gasser: Kortkædede carbonhydrider med lav molekylvægt som methan (CH4), ethan (C2H6) og propan (C3H8) har meget svage intermolekylære kræfter. De er gasser ved stuetemperatur, fordi de har nok energi til at overvinde disse svage attraktioner og bevæge sig frit.
* Væsker: Mellemkædede kulbrinter som butan (C4H10) og pentan (C5H12) har lidt stærkere intermolekylære kræfter på grund af deres større molekylvægt. De er væsker ved stuetemperatur, fordi deres kræfter er stærke nok til at holde dem sammen, men ikke så stærke, at de bliver faste.
* Fast: Langkædede kulbrinter som oktan (C8H18) og højere har betydelig molekylvægt og omfattende overfladeareal. De har stærke intermolekylære kræfter, som kræver høje temperaturer for at overvinde. Det er derfor, de er faste stoffer ved stuetemperatur.
Eksempel:
* Metan (CH4) er en gas, fordi den har en lav molekylvægt og svage London-spredningskræfter.
* Oktan (C8H18) er en væske, fordi den har en større molekylvægt og stærkere London-spredningskræfter.
* Paraffinvoks , et langkædet carbonhydrid, er et fast stof på grund af dets endnu større molekylvægt og meget stærke London-spredningskræfter.
Sammenfattende afhænger et kulbrintes tilstand af en balance mellem styrken af de intermolekylære kræfter, som påvirkes af molekylvægt og forgrening, og temperaturen.
Sidste artikelNatrium- og klorbinding:Ionisk vs. kovalent
Næste artikelForstå opløsningsmidler:Hvad opløser hvad?
 Varme artikler
Varme artikler
-
 IBM annoncerer AI-baseret kemilaboratorium:RoboRXNKredit:Pixabay/CC0 Public Domain IBM har annonceret på sin blogside udviklingen af et AI/cloud-baseret kemilaboratorium ved navn RoboRXN. Dens formål er at hjælpe kemikere med at udvikle nye mat
IBM annoncerer AI-baseret kemilaboratorium:RoboRXNKredit:Pixabay/CC0 Public Domain IBM har annonceret på sin blogside udviklingen af et AI/cloud-baseret kemilaboratorium ved navn RoboRXN. Dens formål er at hjælpe kemikere med at udvikle nye mat -
 Hvordan temperatur påvirker kulsyre i drikkevarerFotokredit:iStock/Getty Images / champlifezy@gmail.com Drik smag og opbevaring Smagsprofilen af kulsyreholdige drikke er stærkt påvirket af deres opbevaringstemperatur. Afkøling af drikkevaren sænker
Hvordan temperatur påvirker kulsyre i drikkevarerFotokredit:iStock/Getty Images / champlifezy@gmail.com Drik smag og opbevaring Smagsprofilen af kulsyreholdige drikke er stærkt påvirket af deres opbevaringstemperatur. Afkøling af drikkevaren sænker -
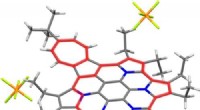 Dobbelt aromatiske ringe stabiliserer multikationerPyrrol- og azulenfusioneret azacoronen-dikering med 22π 6π aromatiske ringe. Kredit:American Chemical Society Et redoxaktivt polycyklisk aromatisk kulbrinte (PAHer) sammensat af azulen og pyrroler
Dobbelt aromatiske ringe stabiliserer multikationerPyrrol- og azulenfusioneret azacoronen-dikering med 22π 6π aromatiske ringe. Kredit:American Chemical Society Et redoxaktivt polycyklisk aromatisk kulbrinte (PAHer) sammensat af azulen og pyrroler -
 Er lim svaret på klimakrisen?Skorstensstak:en harpiks udviklet af et team ved Swansea University kunne hjælpe med at forbedre kulstoffangstmaterialer. Kredit:Veeterzy Er lim svaret på klimaændringer? Forskere ved Energy Safet
Er lim svaret på klimakrisen?Skorstensstak:en harpiks udviklet af et team ved Swansea University kunne hjælpe med at forbedre kulstoffangstmaterialer. Kredit:Veeterzy Er lim svaret på klimaændringer? Forskere ved Energy Safet
- Hvad er produkterne fra neutraliseringsreaktion mellem NHO3 og CA (OH) 2?
- Droner hjælper med at kortlægge Islands forsvindende gletsjere
- Billede:Tricorder
- Forbrugere:Hvorfor kan du lide det, jeg kan lide, men ikke kan lide?
- Hvorfor er bevægelsen af basale elementer i forskellig fra overførselsenergi?
- Hvad kendetegner en Arrhenius syre-base reaktion?


