Natrium- og klorbinding:Ionisk vs. kovalent
* Natrium (Na) er et metal og har en lav ioniseringsenergi, hvilket betyder, at det let mister sin yderste elektron for at blive en positivt ladet ion (Na+).
* Klor (Cl) er et ikke-metal og har en høj elektronaffinitet, hvilket betyder, at det let får en elektron til at blive en negativt ladet ion (Cl-).
Når natrium og klor reagerer, donerer natrium sin elektron til klor. Denne overførsel af elektroner skaber elektrostatisk tiltrækning mellem de modsat ladede ioner, hvilket resulterer i dannelsen af en ionbinding. Den resulterende forbindelse, natriumchlorid (NaCl), er et krystalgitter, der holdes sammen af disse ionbindinger.
Nøgleforskelle mellem kovalente og ioniske bindinger:
* Kovalente bindinger: Indebærer deling af elektroner mellem atomer.
* ioniske bindinger: Indebærer overførsel af elektroner mellem atomer, hvilket resulterer i dannelsen af ioner, der holdes sammen af elektrostatisk tiltrækning.
 Varme artikler
Varme artikler
-
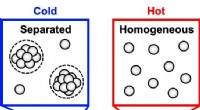 Ny model beskriver faseseparation, der ødelægger antistofopløsningerEn ny undersøgelse brugte en temperaturgradient til at observere, hvor stærkt koncentrerede antistofopløsninger, som dem, der er almindelige i nogle lægemidler, opdelt i faser, som en olie- og vandopl
Ny model beskriver faseseparation, der ødelægger antistofopløsningerEn ny undersøgelse brugte en temperaturgradient til at observere, hvor stærkt koncentrerede antistofopløsninger, som dem, der er almindelige i nogle lægemidler, opdelt i faser, som en olie- og vandopl -
 Kunne vi genbruge plastikposer til fremtidens stoffer?MIT ingeniører har udviklet selvkølende stoffer fra polyethylen, almindeligvis brugt i plastikposer. De vurderer, at det nye stof kan være mere bæredygtigt end bomuld og andre almindelige tekstiler. K
Kunne vi genbruge plastikposer til fremtidens stoffer?MIT ingeniører har udviklet selvkølende stoffer fra polyethylen, almindeligvis brugt i plastikposer. De vurderer, at det nye stof kan være mere bæredygtigt end bomuld og andre almindelige tekstiler. K -
 Kan bionedbrydelige polymerer leve op til hypen?Kredit:Pixabay/CC0 Public Domain Efterhånden som både forbrugere og virksomheder bliver mere miljøbevidste, den kemiske industri arbejder på at finde løsninger på plastikaffaldskrisen. En idé er a
Kan bionedbrydelige polymerer leve op til hypen?Kredit:Pixabay/CC0 Public Domain Efterhånden som både forbrugere og virksomheder bliver mere miljøbevidste, den kemiske industri arbejder på at finde løsninger på plastikaffaldskrisen. En idé er a -
 Prisbillig blysensor til hjemmet, byens vandledningerWen-Chi Lin viser sit elektroniske ledningssensordesign frem. Det kunne gøre det muligt for byer og husejere at lokalisere rør, der forurener vand med bly. Kredit:Evan Dougherty, Michigan Engineering
Prisbillig blysensor til hjemmet, byens vandledningerWen-Chi Lin viser sit elektroniske ledningssensordesign frem. Det kunne gøre det muligt for byer og husejere at lokalisere rør, der forurener vand med bly. Kredit:Evan Dougherty, Michigan Engineering
- Hvordan har vulkanaktivitet påvirket, hvor folk bor i Italien?
- Ny tilgang skaber en enestående enkeltatomskatalysator til vandopdeling
- Sprinklere og drypvanding hjælper irakerne med at slå tørken
- Er isvand et sammensat element eller en blanding?
- Hvordan bruges kobber i en smartphone?
- Hvordan påvirker optisk densitet af et medium hastigheden?


