Massekonservering i løsninger:Forstå loven
1. Loven om bevarelse af masse: Denne grundlæggende lov siger, at stof ikke kan skabes eller ødelægges i almindelige kemiske og fysiske ændringer. Dette betyder, at systemets samlede masse forbliver konstant.
2. Opløsning: Når et opløst stof opløses i et opløsningsmiddel, bliver de opløste molekyler spredt gennem opløsningsmidlet. De opløste molekyler er stadig til stede, bare fordelt anderledes.
3. Ingen ændring i totalmasse: Mens de opløste partikler ikke længere er synlige som en separat fase, er deres masse stadig til stede i opløsningen. Den samlede masse af opløsningen er lig med massen af opløsningsmidlet plus massen af det opløste stof.
Eksempel:
Forestil dig at tilføje 10 gram sukker (opløst stof) til 100 gram vand (opløsningsmiddel).
* Startmasse: 10 gram (sukker) + 100 gram (vand) =110 gram
* Afsluttende masse: 110 gram (sukkeropløsning)
Sukkeropløsningens masse forbliver 110 gram, selvom sukkeret er opløst og ikke længere er synligt adskilt. Sukkermolekylerne er stadig til stede i opløsningen, hvilket bidrager til den samlede masse.
Nøglepunkter:
* Der oprettes ingen nye sager: Opløsningsprocessen involverer ikke at skabe nyt stof. Det ændrer bare, hvordan sagen er fordelt.
* Ingen sag går tabt: De opløste molekyler er simpelthen spredt gennem opløsningsmidlet, men de bidrager stadig til den samlede masse.
Derfor opretholdes bevarelsen af massen, selv når man tilsætter et opløst stof til et opløsningsmiddel. Systemets samlede masse forbliver konstant før og efter opløsningsprocessen.
 Varme artikler
Varme artikler
-
 Beregning af pH-virkningen af fortynding:En praktisk vejledningAf Claire Gillespie Opdateret 30. august 2022 Fortynding er en rutinemæssig laboratorieteknik, som videnskabsstuderende bruger til at opnå præcise koncentrationer. Det sker også i hverdagen - at til
Beregning af pH-virkningen af fortynding:En praktisk vejledningAf Claire Gillespie Opdateret 30. august 2022 Fortynding er en rutinemæssig laboratorieteknik, som videnskabsstuderende bruger til at opnå præcise koncentrationer. Det sker også i hverdagen - at til -
 Ny proces til konservering af tømmer kan give fordele i forhold til trykbehandlingBehandlede og ubehandlede tømmerstykker nedsænket i vand. Tømmeret til venstre er blevet behandlet ved hjælp af atomlagsaflejring. Det modstår at absorbere vand, selv når det er nedsænket. Til højre e
Ny proces til konservering af tømmer kan give fordele i forhold til trykbehandlingBehandlede og ubehandlede tømmerstykker nedsænket i vand. Tømmeret til venstre er blevet behandlet ved hjælp af atomlagsaflejring. Det modstår at absorbere vand, selv når det er nedsænket. Til højre e -
 Maskinlæringsalgoritme hjælper med at søge efter nye lægemidlerKredit:CC0 Public Domain Forskere har designet en maskinlæringsalgoritme til lægemiddelopdagelse, som har vist sig at være dobbelt så effektiv som industristandarden, som kunne fremskynde processe
Maskinlæringsalgoritme hjælper med at søge efter nye lægemidlerKredit:CC0 Public Domain Forskere har designet en maskinlæringsalgoritme til lægemiddelopdagelse, som har vist sig at være dobbelt så effektiv som industristandarden, som kunne fremskynde processe -
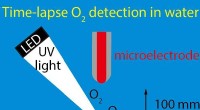 Hurtigere detektion af fotokatalysator-genereret oxygen har store konsekvenser for ren energiFigur 1:Påvisning af oxygen (O2) genereret fra kunstig fotosyntese ved hjælp af en mikroelektrode. Kredit:Kobe University I øjeblikket, størstedelen af den energi, der forbruges af verdens befol
Hurtigere detektion af fotokatalysator-genereret oxygen har store konsekvenser for ren energiFigur 1:Påvisning af oxygen (O2) genereret fra kunstig fotosyntese ved hjælp af en mikroelektrode. Kredit:Kobe University I øjeblikket, størstedelen af den energi, der forbruges af verdens befol
- Er lut en elementblanding eller forbindelse?
- Hvad er naturressourcer?
- Coronavirus er vigtigt, men det er en sand sort svanebegivenhed?
- Hvordan finder du maksimal forskydning i en kraftgraf, der gives indledende og endelig hastighed MAS…
- Koralgartnere bringer Jamaicas rev tilbage, stykke for stykke
- 2 liter svarende til hvor mange liter?


