Klor vs. natriumreaktivitet:Forstå forskellen
* Elektronegativitet: Klor har en højere elektronegativitet end natrium. Det betyder, at klor har en stærkere tiltrækning af elektroner.
* Elektronkonfiguration: Klor har 7 valenselektroner (elektroner i dens yderste skal). Den har brug for en elektron mere for at opnå en stabil oktetkonfiguration. Natrium har på den anden side kun 1 valenselektron. Det er lettere for klor at få en elektron end for natrium at miste en.
* Ioniseringsenergi: Klor har en højere ioniseringsenergi end natrium. Det betyder, at det kræver mere energi at fjerne en elektron fra klor sammenlignet med natrium.
Reaktivitet med hensyn til at få eller tabe elektroner:
* Natrium: Natrium mister let sin ene valenselektron for at opnå en stabil oktetkonfiguration, der danner en positiv ion (Na+). Dette gør det til et stærkt reduktionsmiddel, hvilket betyder, at det nemt kan donere elektroner.
* Klor: Klor får let en elektron for at opnå en stabil oktetkonfiguration, der danner en negativ ion (Cl-). Dette gør det til et stærkt oxidationsmiddel, hvilket betyder, at det nemt accepterer elektroner.
Opsummering: Klorens høje elektronegativitet, tendens til at få elektroner og høje ioniseringsenergi gør det meget mere reaktivt end natrium.
 Varme artikler
Varme artikler
-
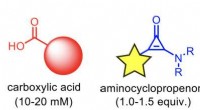 Lysinduceret modifikation af en carboxylsyre med en aminocyclopropenonFotoudløst modifikation af en carboxylsyre ved hjælp af en aminocyclopropenon. Reaktionen afsluttes på kort tid (5-10 min) selv ved lav koncentration (10-20 mM). Modifikationsreaktionen forløber i op
Lysinduceret modifikation af en carboxylsyre med en aminocyclopropenonFotoudløst modifikation af en carboxylsyre ved hjælp af en aminocyclopropenon. Reaktionen afsluttes på kort tid (5-10 min) selv ved lav koncentration (10-20 mM). Modifikationsreaktionen forløber i op -
 Forskere udvikler forbedret genbrugsproces for kulfiberKredit:Unsplash/CC0 Public Domain Genbrug af kompositmaterialer kan være op til 70 procent billigere og føre til en reduktion i CO på 90-95 procent 2 emissioner sammenlignet med standardfremstil
Forskere udvikler forbedret genbrugsproces for kulfiberKredit:Unsplash/CC0 Public Domain Genbrug af kompositmaterialer kan være op til 70 procent billigere og føre til en reduktion i CO på 90-95 procent 2 emissioner sammenlignet med standardfremstil -
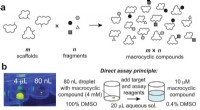 Store antal makrocykliske forbindelser, der er nødvendige for at udvikle lægemidler mod vanskelige…Diversificering af makrocykliske stilladser ved kombinatorisk at tilføje fragmenter til perifere grupper. et generelt princip for tilgangen. b Billede af en 80 nL dråbe overført af ADE, vist i en 96-b
Store antal makrocykliske forbindelser, der er nødvendige for at udvikle lægemidler mod vanskelige…Diversificering af makrocykliske stilladser ved kombinatorisk at tilføje fragmenter til perifere grupper. et generelt princip for tilgangen. b Billede af en 80 nL dråbe overført af ADE, vist i en 96-b -
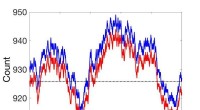 Ikke-steady state massehandlingsdynamik genovervejetSammenligninger mellem ikke-steady state stokastiske kinetiske simuleringer (rød) og simuleringer ved brug af koblet reaktionssætning (blå). Kredit:Pacific Northwest National Laboratory Masseaktio
Ikke-steady state massehandlingsdynamik genovervejetSammenligninger mellem ikke-steady state stokastiske kinetiske simuleringer (rød) og simuleringer ved brug af koblet reaktionssætning (blå). Kredit:Pacific Northwest National Laboratory Masseaktio
- Kan vindkraft arbejde med andre former for energi?
- Bioinspirerede strategier til udvikling af nye lægemidler
- Vådsæsonændringer under fremtidige klimaændringer kan skade sårbart Afrika
- Hvilken metamorfe klippe, der i vid udstrækning blev brugt til monumenter og bygninger, ville forvæ…
- Hvilken dosis loven om bevaringsenergi forklarer?
- Hvad er måling af gravitationskraft mellem Jorden og et objekt?


