Kovalente bindinger:Forståelse af elektrondeling og kemisk stabilitet
Her er en oversigt over nøglepunkter:
* Deling af elektroner: I modsætning til ionbindinger, hvor et atom donerer en elektron til et andet, involverer kovalente bindinger gensidig deling af elektroner.
* Stabil elektronkonfiguration: Atomer ønsker at have en fuld ydre skal af elektroner for stabilitet. Ved at dele elektroner kan atomer opnå denne stabile konfiguration og opfylde oktetreglen (bortset fra brint, som kun har brug for 2 elektroner).
* Typer af kovalente bindinger:
* Ikke-polære kovalente bindinger: Elektroner deles ligeligt mellem de to atomer. Dette sker, når de to atomer har lignende elektronegativitet (evne til at tiltrække elektroner).
* Polære kovalente bindinger: Elektroner deles ulige. Dette sker, når det ene atom har en højere elektronegativitet end det andet, hvilket fører til en delvis positiv og delvis negativ ladning på atomerne.
* Styrke af kovalente bindinger: Kovalente bindinger er generelt stærke, hvilket gør de molekyler, de danner, relativt stabile. Styrken af en kovalent binding afhænger af antallet af delte elektroner og de involverede typer atomer.
Eksempler:
* Vand (H₂O): Oxygen deler to elektroner med hvert brintatom og danner to polære kovalente bindinger.
* Metan (CH₄): Kulstof deler en elektron med hver af de fire brintatomer og danner fire ikke-polære kovalente bindinger.
* Nitrogengas (N₂): Hvert nitrogenatom deler tre elektroner med det andet og danner en tredobbelt kovalent binding.
Nøgleforskelle fra ioniske bindinger:
* Ionbindinger: involverer overførsel af elektroner, der danner ioner (ladede atomer), der holdes sammen af elektrostatisk tiltrækning.
* Kovalente bindinger: involverer deling af elektroner, hvilket resulterer i neutrale molekyler holdt sammen af det delte elektronpar.
Kovalente bindinger er grundlaget for mange organiske molekyler og spiller en afgørende rolle i livets struktur og funktion.
Sidste artikelForstå FeC2H3O23:Hvorfor denne formel er ugyldig
Næste artikelKoboltanvendelser:Vigtige industrielle anvendelser og egenskaber
 Varme artikler
Varme artikler
-
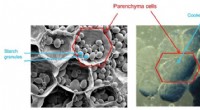 Ny forarbejdningsteknik kan gøre kartofler sundereMikroskopisk billede af kartoffelvæv før (venstre) og efter (højre) kogning eller forarbejdning. Kredit:Amy Lin, A*STAR, og Yijing Shao og YuLian Lin, University of Idaho. Forskere annoncerede tidl
Ny forarbejdningsteknik kan gøre kartofler sundereMikroskopisk billede af kartoffelvæv før (venstre) og efter (højre) kogning eller forarbejdning. Kredit:Amy Lin, A*STAR, og Yijing Shao og YuLian Lin, University of Idaho. Forskere annoncerede tidl -
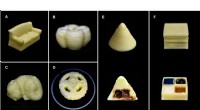 Forskere udvikler en enkel metode til 3-D-print af mælkeprodukterA - D:3D-printede mælkestrukturer af sofa, fæstning, hjul, og kløverblad, henholdsvis. E:3D-printet kegle indeholdende flydende chokoladesirup som internt fyld.F:3D-printet terning med fire rum indeho
Forskere udvikler en enkel metode til 3-D-print af mælkeprodukterA - D:3D-printede mælkestrukturer af sofa, fæstning, hjul, og kløverblad, henholdsvis. E:3D-printet kegle indeholdende flydende chokoladesirup som internt fyld.F:3D-printet terning med fire rum indeho -
 For en sand krig mod affald, modeindustrien skal bruge mere på forskningEn model bærer et af forfatterens originale zero waste designs. Stigningen af fast fashion i Australien betyder, at 6000 kg tøj bliver dumpet på lossepladsen hvert 10. minut. ABCs War On Waste v
For en sand krig mod affald, modeindustrien skal bruge mere på forskningEn model bærer et af forfatterens originale zero waste designs. Stigningen af fast fashion i Australien betyder, at 6000 kg tøj bliver dumpet på lossepladsen hvert 10. minut. ABCs War On Waste v -
 Aske fra kraftværker forarbejdet til reagenser til vandrensningKredit:CC0 Public Domain Russiske metallurger har foreslået at opløse askeaffaldet fra termiske kraftværker med saltsyre ved højt tryk. De resulterende forbindelser kan anvendes til vandbehandling
Aske fra kraftværker forarbejdet til reagenser til vandrensningKredit:CC0 Public Domain Russiske metallurger har foreslået at opløse askeaffaldet fra termiske kraftværker med saltsyre ved højt tryk. De resulterende forbindelser kan anvendes til vandbehandling
- Ulighederne ved en pandemi:Spaniens illustration af socioøkonomisk sårbarhed og sygdom
- Hvad er det multicellulære videnskabelige navn?
- Blockchain-systemer sporer fødevaresikkerhed og oprindelse
- Kun spise østers i måneder med et 'r'? Tommelfingerregel er mindst 4.000 år gammel
- Gendannelse af tabte dimensioner af billeder og video
- Afdelingen for geologisk tid, der udgør omkring 88 procent historie kaldes?


