Forstå surheden af trichloreddikesyre (TCA) vs. dichloreddikesyre og monochloreddikesyre
Her er en oversigt over hvorfor:
* Induktiv effekt: Klor er mere elektronegativt end kulstof og brint. Dette betyder, at kloratomer trækker elektrontætheden væk fra det carbonatom, de er knyttet til. Denne elektrontiltrækkende effekt kaldes den induktive effekt.
* Stabilisering af konjugatbasen: Når en carboxylsyre mister en proton (H+), danner den en carboxylatanion (RCOO-). Jo mere stabil konjugatbasen er, jo stærkere er syren.
* Trichloreddikesyre: I trichloreddikesyre udøver tre chloratomer en stærk induktiv effekt på carboxylatanionen, trækker elektrondensiteten tilbage og stabiliserer den negative ladning. Dette gør konjugatbasen mere stabil og syren stærkere.
* Dichloreddikesyre: Dichloreddikesyre har to kloratomer, hvilket fører til en svagere induktiv effekt sammenlignet med trichloreddikesyre. Dette resulterer i en mindre stabil konjugeret base og en svagere syre.
* Monochloreddikesyre: Monochloreddikesyre har kun ét kloratom, hvilket resulterer i den svageste induktive effekt blandt de tre. Følgelig er dens konjugerede base den mindst stabile, hvilket gør den til den svageste syre.
Opsummering: Jo flere kloratomer der er til stede på eddikesyremolekylet, jo stærkere er den induktive effekt, hvilket fører til en mere stabil konjugeret base og en stærkere syre.
 Varme artikler
Varme artikler
-
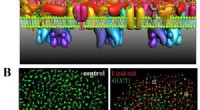 Super-opløsning billeddannelse afslører mekanisme af GLUT1 klyngedannelseA) Dette er PLLPI-modellen af cellemembranen. B) dSTORM-billeder af GLUT1 på cellemembranen; GLUT1 og lipid rafts; og GLUT1-fordeling efter MβCD- og NaN3-behandling. Skala barer, 5 μm. Kredit:GAO Ji
Super-opløsning billeddannelse afslører mekanisme af GLUT1 klyngedannelseA) Dette er PLLPI-modellen af cellemembranen. B) dSTORM-billeder af GLUT1 på cellemembranen; GLUT1 og lipid rafts; og GLUT1-fordeling efter MβCD- og NaN3-behandling. Skala barer, 5 μm. Kredit:GAO Ji -
 Hvordan farveskiftende kemiske reaktioner afslører skjult molekylær dynamikAf Claire Gillespie, Opdateret Aug302022 Grafner/iStock/GettyImages En kemisk reaktion er ikke altid synlig for det blotte øje, men nogle producerer dramatiske farveændringer, der gør eksperimenter
Hvordan farveskiftende kemiske reaktioner afslører skjult molekylær dynamikAf Claire Gillespie, Opdateret Aug302022 Grafner/iStock/GettyImages En kemisk reaktion er ikke altid synlig for det blotte øje, men nogle producerer dramatiske farveændringer, der gør eksperimenter -
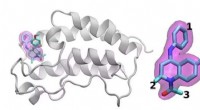 Forskningsgruppen bruger supercomputing til at målrette de mest lovende lægemiddelkandidater ud fr…En skematisk oversigt over BRD4 -proteinet bundet til et af 16 lægemidler baseret på det samme tetrahydroquinolin -stillads (fremhævet i magenta). Regioner, der er kemisk modificeret mellem de lægemid
Forskningsgruppen bruger supercomputing til at målrette de mest lovende lægemiddelkandidater ud fr…En skematisk oversigt over BRD4 -proteinet bundet til et af 16 lægemidler baseret på det samme tetrahydroquinolin -stillads (fremhævet i magenta). Regioner, der er kemisk modificeret mellem de lægemid -
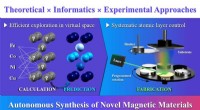 Mod autonom forudsigelse og syntese af nye magnetiske materialerKredit:Tokyo University of Science I materialevidenskab udforskes kandidater til nye funktionelle materialer normalt på en trial-and-error måde gennem beregninger, syntetiske metoder og materialean
Mod autonom forudsigelse og syntese af nye magnetiske materialerKredit:Tokyo University of Science I materialevidenskab udforskes kandidater til nye funktionelle materialer normalt på en trial-and-error måde gennem beregninger, syntetiske metoder og materialean


