Aluminiumsproduktion:Reaktion af aluminiumoxid med kulilte
Reaktionen:
* Aluminiumoxid (Al₂O₃) (fast) + Kulilte (CO) (gas) → Aluminium (Al) (fast) + Kuldioxid (CO₂) (gas)
Forklaring:
* Aluminiumoxid (Al₂O₃) er en meget stabil forbindelse, hvilket gør det svært at udvinde aluminium direkte fra det.
* Kulmonoxid (CO) virker som et reduktionsmiddel. Det betyder, at den "donerer" elektroner til aluminiumet i aluminiumoxid, hvilket får det til at miste sin ilt og bliver til rent aluminium.
* Aluminium (Al) er det ønskede produkt, et let og alsidigt metal.
* Culdioxid (CO₂) er et biprodukt af reaktionen.
Processen:
Denne reaktion udføres i en proces kaldet Hall-Héroult-processen . Her er en forenklet oversigt:
1. Elektrolyse: Aluminiumoxid er opløst i smeltet kryolit (Na₃AlF6), et mineral, der sænker oxidets smeltepunkt.
2. Elektroder: Den smeltede blanding anbringes i en beholder med kulelektroder.
3. Reduktion: En elektrisk strøm ledes gennem blandingen, hvilket får kulilte til at reducere aluminiumoxidet til aluminiummetal.
4. Samling: Aluminiummetal samler sig i bunden af beholderen.
Vigtig bemærkning: Denne reaktion er meget energikrævende på grund af det høje smeltepunkt af aluminiumoxid. Hall-Héroult-processen er dog den primære metode til fremstilling af aluminium i stor skala.
Sidste artikelGrundstoffer i svovlsyre (H₂SO4):En simpel forklaring
Næste artikelDannelse af sur regn:Hvordan svovldioxid skaber svovlsyre
 Varme artikler
Varme artikler
-
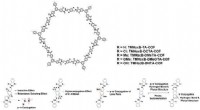 Redigering af lysemitterende organiske molekyler via overflademodifikationFigur 1. Ændringer i lysemission via forstyrrelse af vægoverfladesteder i kovalente organiske rammer (COFer). Ved at introducere forskellige atomer eller små grupper i porestederne af hydrazon-forbund
Redigering af lysemitterende organiske molekyler via overflademodifikationFigur 1. Ændringer i lysemission via forstyrrelse af vægoverfladesteder i kovalente organiske rammer (COFer). Ved at introducere forskellige atomer eller små grupper i porestederne af hydrazon-forbund -
 Sådan fungerer ozongeneratorer:Videnskab, applikationer og sikkerhedsstandarderIgor Alecsander/iStock/GettyImages Hvad er ozon? Ozon (O3 ) er en meget reaktiv form for oxygen. I modsætning til det diatomiske O2 , ozon består af tre oxygenatomer. Det ekstra atom er svagt bundet,
Sådan fungerer ozongeneratorer:Videnskab, applikationer og sikkerhedsstandarderIgor Alecsander/iStock/GettyImages Hvad er ozon? Ozon (O3 ) er en meget reaktiv form for oxygen. I modsætning til det diatomiske O2 , ozon består af tre oxygenatomer. Det ekstra atom er svagt bundet, -
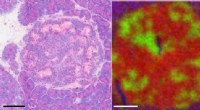 Kortlægning af kræftbevægelserKræftforskere kæmper for at identificere tumorceller, der er spredt i ikke-maligne væv, fordi tumorceller udnytter vævsmiljøet og monopoliserer tilgængelige ressourcer for at fortsætte med at vokse. F
Kortlægning af kræftbevægelserKræftforskere kæmper for at identificere tumorceller, der er spredt i ikke-maligne væv, fordi tumorceller udnytter vævsmiljøet og monopoliserer tilgængelige ressourcer for at fortsætte med at vokse. F -
 En ny strategi til at stabilisere carbonnitrid-fotokatalysator til nitrogenreduktion(a) TEM-billede af BCN; (b) UV-vis diffuse reflektansspektre, (c) steady-state PL-spektre, (d) forbigående fotostrømresponser og (e) N2-TPD af CN og BCN; (f) MD-simuleringssnapshots af BCN. Kredit:WAN
En ny strategi til at stabilisere carbonnitrid-fotokatalysator til nitrogenreduktion(a) TEM-billede af BCN; (b) UV-vis diffuse reflektansspektre, (c) steady-state PL-spektre, (d) forbigående fotostrømresponser og (e) N2-TPD af CN og BCN; (f) MD-simuleringssnapshots af BCN. Kredit:WAN
- Nanopore-teknologi opnår gennembrud inden for påvisning af proteinvarianter
- Hvad er lava, og hvordan flyder det?
- Hvor sandsynligt er det, at engelske elever tager eksamen fra gymnasiet? Undersøgelse viser, at det…
- Hvad indeholder metaller, der gør dem til gode ledere?
- Hvad består af en cellekropsdendritter og axon?
- Hvor kommer Maryland krabber fra? Forskere bruger en virus, havstrømskort og mere til at finde ud a…


