Elektrolyse:Forståelse af processen med kemisk bindingsnedbrydning
Her er en oversigt:
* Elektrolyse er en kemisk proces, hvor en elektrisk strøm føres gennem et stof, hvilket forårsager en kemisk ændring.
* Denne strøm giver den nødvendige energi til at bryde de kemiske bindinger i stoffet.
* Brydningen af disse bindinger resulterer i dannelsen af nye stoffer.
Nøglepunkter om elektrolyse:
* Elektroder: Elektrolyse udføres ved hjælp af elektroder, som normalt er lavet af inerte materialer som platin eller kulstof. Disse elektroder leder elektricitet og tjener som de punkter, hvor den elektriske strøm kommer ind og forlader stoffet.
* Elektrolyt: Stoffet, der gennemgår elektrolyse, er typisk opløst i en væske kaldet en elektrolyt. Elektrolytter er opløsninger eller smeltede forbindelser, der leder elektricitet på grund af tilstedeværelsen af ioner.
* Redox-reaktioner: Elektrolyse involverer redoxreaktioner. Ved anoden sker der oxidation (tab af elektroner). Ved katoden sker der reduktion (forstærkning af elektroner).
* Applikationer: Elektrolyse har mange anvendelser, herunder:
* Galvanisering: Belægning af en metalgenstand med et andet metal.
* Produktion af klorgas: Anvendes til desinfektionsmidler og plastproduktion.
* Produktion af aluminium: Udvinding af aluminium fra sin malm.
* Produktion af brint: Anvendes som rent brændstof.
Eksempel:
Elektrolyse af vand er et klassisk eksempel. Når en elektrisk strøm ledes gennem vand, nedbrydes vandmolekylerne til brint og iltgas:
* 2H2O(l) → 2H2(g) + O2(g)
I denne reaktion giver den elektriske strøm den nødvendige energi til at bryde bindingerne mellem brint- og oxygenatomer i vandmolekyler. Hydrogen- og oxygenatomerne rekombinerer derefter for at danne henholdsvis hydrogengas og oxygengas.
Lad mig vide, hvis du vil have flere detaljer om et specifikt aspekt af elektrolyse!
 Varme artikler
Varme artikler
-
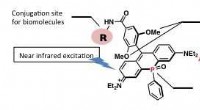 Et nær-infrarødt fluorescerende farvestof til langsigtet biobilleddannelseMolekylær struktur af det nye nær-infrarøde fluorescerende mærkningsmiddel PREX 710 med et koblingssted for et biomolekyle. Inkorporering af den elektrontiltrækkende phosphinoxid (P=O)-del i xanthenst
Et nær-infrarødt fluorescerende farvestof til langsigtet biobilleddannelseMolekylær struktur af det nye nær-infrarøde fluorescerende mærkningsmiddel PREX 710 med et koblingssted for et biomolekyle. Inkorporering af den elektrontiltrækkende phosphinoxid (P=O)-del i xanthenst -
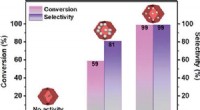 Et katalytisk system af uædle metaller til højeffektiv hydrogenering af nitroarenerKatalytisk ydeevne af katalysatorer med forskellige Zn/Co-forhold. Kredit:TIAN Hao En forskergruppe ledet af prof. LIU Jian fra Dalian Institute of Chemical Physics (DICP) ved det kinesiske videns
Et katalytisk system af uædle metaller til højeffektiv hydrogenering af nitroarenerKatalytisk ydeevne af katalysatorer med forskellige Zn/Co-forhold. Kredit:TIAN Hao En forskergruppe ledet af prof. LIU Jian fra Dalian Institute of Chemical Physics (DICP) ved det kinesiske videns -
 Beregning af ligevægtstryk:En trin-for-trin guideAf Lee Johnson • Opdateret 24. marts 2022 Kemisk ligevægt beskriver den stabile tilstand af en reversibel reaktion, hvor reaktanter omdannes til produkter og omvendt med lige store hastigheder. I pra
Beregning af ligevægtstryk:En trin-for-trin guideAf Lee Johnson • Opdateret 24. marts 2022 Kemisk ligevægt beskriver den stabile tilstand af en reversibel reaktion, hvor reaktanter omdannes til produkter og omvendt med lige store hastigheder. I pra -
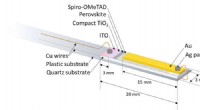 Lyser på, hvad der virkelig sker i perovskit-solcellerSkematisk struktur af elektriske kontakter og ledninger af perovskit-solcellen i et ESR-prøverør. Kredit:University of Tsukuba Forbrugere verden over efterspørger grønnere energikilder; derfor, op
Lyser på, hvad der virkelig sker i perovskit-solcellerSkematisk struktur af elektriske kontakter og ledninger af perovskit-solcellen i et ESR-prøverør. Kredit:University of Tsukuba Forbrugere verden over efterspørger grønnere energikilder; derfor, op
- Hvilken energi, der ikke forårsager nogen ændringer nu, men kan forårsage i fremtiden?
- NASA giver et afskedsinfrarødt billede af den ekstratropiske storm Melissa
- Årstiderne skifter:Forskere giver en ny definition af den store indiske monsunsæson
- Undersøgelse afslører insiderhandel på det australske aktiemarked
- Hotspot-opdagelse beviser canadiske astrofysikere sort hul-teori
- NASA vælger instrument til fremtidig international mission til Mars måner


