Elektrolytdissociation i vand:Forståelse af processen
1. Dissociation:
* De ioniske bindinger, der holder elektrolytten sammen, brydes.
* De enkelte ioner (kationer og anioner) bliver omgivet af vandmolekyler og danner det, der kaldes en hydreringsskal.
* Denne proces kaldes dissociation .
2. Ledningsevne:
* Tilstedeværelsen af frie ioner i opløsningen tillader strømmen af elektrisk strøm.
* Det er derfor elektrolytter leder elektricitet.
3. Kolligative egenskaber:
* Tilstedeværelsen af opløste ioner påvirker opløsningens følgende egenskaber:
* Damptrykssænkning: Opløsningens damptryk falder sammenlignet med rent vand.
* Kogepunktshøjde: Opløsningens kogepunkt stiger sammenlignet med rent vand.
* Frysepunktsdepression: Opløsningens frysepunkt falder sammenlignet med rent vand.
* Osmotisk tryk: Det osmotiske tryk af opløsningen stiger sammenlignet med rent vand.
4. Kemiske reaktioner:
* De opløste ioner kan deltage i kemiske reaktioner.
* Dette er vigtigt i mange biologiske processer, såsom nerveimpulser og muskelsammentrækninger.
5. pH-ændringer:
* Tilsætning af elektrolytter kan påvirke opløsningens pH.
* For eksempel dissocierer stærke syrer og baser fuldstændigt i vand, hvilket fører til betydelige pH-ændringer.
Samlet set resulterer tilsætning af ionisk bundne elektrolytter til vand i en opløsning med:
* Øget ledningsevne
* Ændrede kolligative egenskaber
* Potentiale for kemiske reaktioner
* Mulige pH-ændringer
De specifikke virkninger afhænger af elektrolyttens beskaffenhed (dens styrke, koncentration og kemiske egenskaber).
 Varme artikler
Varme artikler
-
 Mestring af konverteringsfaktorer i kemiske formler:En praktisk vejledningI kemi repræsenterer subscripts i formler kvantitative forhold, ikke kun symboler. Hvert subscript koder for en konverteringsfaktor, der forbinder elementer, molekyler og målbare mængder. At forstå di
Mestring af konverteringsfaktorer i kemiske formler:En praktisk vejledningI kemi repræsenterer subscripts i formler kvantitative forhold, ikke kun symboler. Hvert subscript koder for en konverteringsfaktor, der forbinder elementer, molekyler og målbare mængder. At forstå di -
 Forskere udvikler materiale, der kan regenerere tandemaljenNærbillede af det emaljeagtige materiale. Kredit:Alvaro Mata Forskere ved Queen Mary University of London har udviklet en ny måde at dyrke mineraliserede materialer på, som kan regenerere hårdt væ
Forskere udvikler materiale, der kan regenerere tandemaljenNærbillede af det emaljeagtige materiale. Kredit:Alvaro Mata Forskere ved Queen Mary University of London har udviklet en ny måde at dyrke mineraliserede materialer på, som kan regenerere hårdt væ -
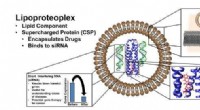 Forskere skaber biomateriale, der leverer både et kraftfuldt lægemiddel og gendæmpereLipoproteoplex bruger en lipid-beholder til transfektion - transport af materiale forbi en cellemembran - og en proteinkapsel, der er nem at fremstille, der kan binde både små molekyle kemoterapeutisk
Forskere skaber biomateriale, der leverer både et kraftfuldt lægemiddel og gendæmpereLipoproteoplex bruger en lipid-beholder til transfektion - transport af materiale forbi en cellemembran - og en proteinkapsel, der er nem at fremstille, der kan binde både små molekyle kemoterapeutisk -
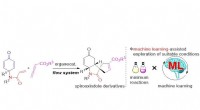 En vanskelig reaktionssekvens får et stort løft fra et flow-opsætning og statistikMaskinstøttet udforskning af organokatalyseret dominoreaktion i flowsystem. Kredit:Royal Society of Chemistry Forskere fra Osaka University optimerer en kompliceret dominoreaktion i et flowsystem
En vanskelig reaktionssekvens får et stort løft fra et flow-opsætning og statistikMaskinstøttet udforskning af organokatalyseret dominoreaktion i flowsystem. Kredit:Royal Society of Chemistry Forskere fra Osaka University optimerer en kompliceret dominoreaktion i et flowsystem
- Hvor hurtigt rejste Apollo til månen?
- EU beklager dybt tilbagetrækning af den amerikanske klimapagt i Paris
- Ny indsigt styrker Einsteins idé om, hvordan varme bevæger sig gennem faste stoffer
- Lazy snyderi lever under jorden,
- Pludselig undviger du huller efter al denne regn? Her er hvordan droner kunne hjælpe med reparation…
- 3-D bioprint af levende strukturer med indbyggede kemiske sensorer


