Forståelse af høje temperaturer i industrielle reaktioner:fordele og mekanismer
1. Øget reaktionsrate:
* Kinetisk energi: Højere temperaturer betyder, at molekyler har mere kinetisk energi, hvilket fører til hyppigere og mere energiske kollisioner. Denne øgede kollisionsfrekvens og energi øger reaktionshastigheden markant.
* Aktiveringsenergi: Mange reaktioner har en aktiveringsenergibarriere, som skal overvindes, for at reaktionen kan fortsætte. Høje temperaturer giver den nødvendige energi til at overvinde denne barriere.
2. Ligevægtsskift:
* Endotermiske reaktioner: For endoterme reaktioner (reaktioner, der absorberer varme), forskyder en forøgelse af temperaturen ligevægten mod produkterne, hvilket fremmer produktdannelsen.
3. Forbedret effektivitet:
* Hurtigere reaktionstid: Høje temperaturer fører til hurtigere reaktioner, hvilket giver mulighed for højere gennemløb og hurtigere produktionshastigheder.
* Forbedret produktudbytte: Ved at øge reaktionshastigheden og skifte ligevægt kan høje temperaturer øge udbyttet af ønskede produkter.
4. Faseændring:
* Smeltning og fordampning: Nogle industrielle processer kræver, at reaktanter er i flydende eller gasformig tilstand, hvilket kan opnås ved at opvarme dem til deres smelte- eller kogepunkt.
5. Katalysatoroptimering:
* Katalysatoraktivitet: Mange industrielle reaktioner anvender katalysatorer til at accelerere reaktionen. Katalysatoraktivitet er ofte temperaturafhængig, og optimal ydeevne kan kræve høje temperaturer.
Der er dog også ulemper ved at udføre reaktioner ved høje temperaturer:
* Øgede energiomkostninger: Opvarmning kræver et betydeligt energiforbrug, hvilket øger produktionsomkostningerne.
* Sikkerhedsbekymringer: Høje temperaturer kan udgøre sikkerhedsrisici på grund af potentielle eksplosioner, brande og beskadigelse af udstyr.
* Sidereaktioner: Forhøjede temperaturer kan føre til uønskede bivirkninger, hvilket reducerer udbyttet af ønskede produkter.
Samlet set indebærer beslutningen om at udføre en reaktion ved høj temperatur en omhyggelig balance mellem fordele og ulemper. Den optimale temperatur for en specifik reaktion afhænger af faktorer som reaktionskinetik, termodynamik, katalysatoraktivitet og sikkerhedsovervejelser.
Sidste artikelMetaloxidation:Forståelse af metaloxiddannelse
Næste artikelKlor-hydrogenbinding:Forståelse af kovalent binding
 Varme artikler
Varme artikler
-
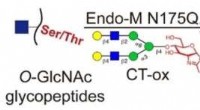 Reversibel kemoenzymatisk mærkningsstrategi muliggør dybdegående analyse af protein O-GlcNAcyleri…Kredit:Angewandte Chemie (2022). DOI:10.1002/ange.202117849 O-bundet β-N-acetylglucosamin (O-GlcNAcylation), en vigtig post-translationel modifikation (PTM) af proteiner, er involveret i forskellig
Reversibel kemoenzymatisk mærkningsstrategi muliggør dybdegående analyse af protein O-GlcNAcyleri…Kredit:Angewandte Chemie (2022). DOI:10.1002/ange.202117849 O-bundet β-N-acetylglucosamin (O-GlcNAcylation), en vigtig post-translationel modifikation (PTM) af proteiner, er involveret i forskellig -
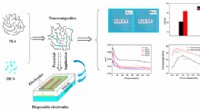
 Effektiv og high-throughput teknik til at studere strukturen af DNAFra venstre mod højre:SEM-billede af DNA-bundter homogent suspenderet over en superhydrofob enhed. I det relaterede HRTEM-billede har frynserne en afstand på 2,7 Å, i god overensstemmelse med diffrakt
Effektiv og high-throughput teknik til at studere strukturen af DNAFra venstre mod højre:SEM-billede af DNA-bundter homogent suspenderet over en superhydrofob enhed. I det relaterede HRTEM-billede har frynserne en afstand på 2,7 Å, i god overensstemmelse med diffrakt -
 Ny forskning viser, hvordan grupperede partikler bestemmer elasticiteten af nogle gelerEt team af forskere, herunder UDs Eric Furst, opdagede, at gelernes elasticitet stammer fra pakning af klynger af partikler i gelerne, som gruppen kaldte lokalt glasagtige klynger. Kredit:Eric Furst,
Ny forskning viser, hvordan grupperede partikler bestemmer elasticiteten af nogle gelerEt team af forskere, herunder UDs Eric Furst, opdagede, at gelernes elasticitet stammer fra pakning af klynger af partikler i gelerne, som gruppen kaldte lokalt glasagtige klynger. Kredit:Eric Furst, -
 Nedbrydelige elektroniske komponenter fremstillet af majsstivelseKredit:American Chemical Society Efterhånden som forbrugerne opgraderer deres gadgets i et stigende tempo, mængden af elektronisk affald, vi genererer, fortsætter med at stige. For at hjælpe med
Nedbrydelige elektroniske komponenter fremstillet af majsstivelseKredit:American Chemical Society Efterhånden som forbrugerne opgraderer deres gadgets i et stigende tempo, mængden af elektronisk affald, vi genererer, fortsætter med at stige. For at hjælpe med
- Hvad deler de indre og ydre planter?
- Ændres lysenergi til celle i fase 1 af fotosyntesen?
- Er friktionskraften, der fungerer på genstande, ikke bevæger sig?
- Voksende klimaangst udgør en betydelig trussel mod individer og samfund
- Hvad er forskellen mellem en klit og en bakke?
- Medarbejdere føler sig brændt over brudte løfter om at arbejde hjemmefra, virksomhedskultur BS


