Forståelse af ammoniak-likvefaktion:intermolekylære kræfter og betingelser
* Stærke intermolekylære kræfter: Ammoniak (NH3) molekyler er polære, hvilket betyder, at de har en positiv og en negativ ende på grund af elektronegativitetsforskellen mellem nitrogen og brint. Denne polaritet giver mulighed for stærke dipol-dipol-interaktioner mellem molekyler. Derudover kan ammoniak danne brintbindinger, som er endnu stærkere intermolekylære kræfter.
* Tryk og temperatur:
* Tryk: Forøgelse af trykket tvinger molekylerne tættere sammen, hvilket øger styrken af de intermolekylære kræfter.
* Temperatur: Sænkning af temperaturen reducerer molekylernes kinetiske energi, hvilket gør det lettere for de intermolekylære kræfter at overvinde molekylernes bevægelse og holde dem sammen i flydende tilstand.
Liquefaction Process:
Når ammoniakgas udsættes for både øget tryk og reduceret temperatur, sker følgende:
1. Molekylerne bremser på grund af den lavere temperatur.
2. Det øgede tryk tvinger molekylerne tættere sammen.
3. De stærke intermolekylære kræfter bliver dominerende og overvinder molekylernes kinetiske energi.
4. Gasmolekylerne går over i en mere kondenseret, flydende tilstand.
Opsummeret bliver ammoniakgas flydende på grund af kombinationen af stærke intermolekylære kræfter (dipol-dipol og hydrogenbinding) og gunstige betingelser for tryk og temperatur.
 Varme artikler
Varme artikler
-
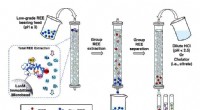 Ny, miljøvenlig metode til at udvinde og adskille sjældne jordarterLavkvalitetskilder til sjældne jordarters grundstoffer (REE), fra industriaffald, indeholder typisk mange sjældne jordarters grundstoffer og andre metaller blandet sammen. En ny ekstraktions- og separ
Ny, miljøvenlig metode til at udvinde og adskille sjældne jordarterLavkvalitetskilder til sjældne jordarters grundstoffer (REE), fra industriaffald, indeholder typisk mange sjældne jordarters grundstoffer og andre metaller blandet sammen. En ny ekstraktions- og separ -
 Fremstilling af mikrober, der omdanner drivhusgasserUSF-forsker Alex Chou manipulerer DNA for at konstruere E. coli til C1-konvertering. Kredit:University of South Florida Forskere ved University of South Florida udnytter kraften i den menneskelige
Fremstilling af mikrober, der omdanner drivhusgasserUSF-forsker Alex Chou manipulerer DNA for at konstruere E. coli til C1-konvertering. Kredit:University of South Florida Forskere ved University of South Florida udnytter kraften i den menneskelige -
 Ny metode fremskynder udviklingen af medicinI laboratoriet hos Bernhard Spingler (r.), praktikant Philipp Nievergelt (l.) ydede et vigtigt bidrag til hurtigere og lettere at bestemme krystalstrukturerne af organiske salte. Kredit:UZH Forske
Ny metode fremskynder udviklingen af medicinI laboratoriet hos Bernhard Spingler (r.), praktikant Philipp Nievergelt (l.) ydede et vigtigt bidrag til hurtigere og lettere at bestemme krystalstrukturerne af organiske salte. Kredit:UZH Forske -
 Ny produktionsteknik til højtydende polymer kunne give bedre rustningEn ny katalysator fremstillet af legerede nanopartikler af guld og palladium kan producere PBO-polymer, som bruges i kropsrustninger og andre højtydende stoffer. Den nye katalysator producerer PBO, de
Ny produktionsteknik til højtydende polymer kunne give bedre rustningEn ny katalysator fremstillet af legerede nanopartikler af guld og palladium kan producere PBO-polymer, som bruges i kropsrustninger og andre højtydende stoffer. Den nye katalysator producerer PBO, de
- Stadier af økologisk rækkefølge
- USDA spreder rabiesvacciner til dyreliv i 13 stater
- Nyt antibiotikum giver et slag mod bakteriel resistens
- En ny online-beregner estimerer den sande værdi af aktier hos venture-støttede startups
- Sådan finder du en konus radius
- Hvilke ujævne kræfter, der virker på partiklerne på en overflade?


