Boyles lov forklaret:Gastryk og volumenforhold
Her er hvorfor:
* Omvendt proportionalitet: Det betyder, at når trykket stiger, falder volumen, og omvendt, mens produktet af tryk og volumen holdes konstant.
* Konstant temperatur: Hvis temperaturen ændres, vil gasmolekylerne bevæge sig hurtigere eller langsommere, hvilket påvirker deres kollisioner med beholdervæggene og ændrer trykket.
* Konstant mængde gas: Hvis mængden af gas ændres, ændres antallet af molekyler, der kolliderer med beholdervæggene, hvilket påvirker trykket.
Sammenfattende gælder Boyles lov kun, når temperaturen og mængden af gas holdes konstant.
Sidste artikelHydrogenbindinger i DNA og RNA:Forståelse af baseparring
Næste artikelKuldioxid (CO2):Kovalente bindinger forklaret
 Varme artikler
Varme artikler
-
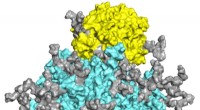 Ofte overset, molekyler kaldet glykaner regulerer COVID-19-spidsproteinfunktionenEn molekylær model viser det stærkt glykosylerede SARS-CoV-2-spidsprotein (cyan, med glykaner i grå og andre farver) bundet til den cellulære ACE2-receptor (gul). En ny undersøgelse fremhæver den krit
Ofte overset, molekyler kaldet glykaner regulerer COVID-19-spidsproteinfunktionenEn molekylær model viser det stærkt glykosylerede SARS-CoV-2-spidsprotein (cyan, med glykaner i grå og andre farver) bundet til den cellulære ACE2-receptor (gul). En ny undersøgelse fremhæver den krit -
 Tynde lag vand lover løfte om fremtidens energilagringLavtemperatur høj opløsning transmissionselektronmikroskop billede af en trombocyt af wolframoxiddihydrat; striberne er individuelle lag af atomer adskilt af vandlag. Kredit:North Carolina State Unive
Tynde lag vand lover løfte om fremtidens energilagringLavtemperatur høj opløsning transmissionselektronmikroskop billede af en trombocyt af wolframoxiddihydrat; striberne er individuelle lag af atomer adskilt af vandlag. Kredit:North Carolina State Unive -
 Hvorfor saltvand fremskynder metalrustning:Videnskaben bag korrosionAf Claire Gillespie | Opdateret 24. marts 2022 Jernoxid - almindeligvis kaldet rust - er en rødbrun forbindelse, der dannes, når jern reagerer med ilt i nærvær af vand eller fugt. Når chloridioner
Hvorfor saltvand fremskynder metalrustning:Videnskaben bag korrosionAf Claire Gillespie | Opdateret 24. marts 2022 Jernoxid - almindeligvis kaldet rust - er en rødbrun forbindelse, der dannes, når jern reagerer med ilt i nærvær af vand eller fugt. Når chloridioner -
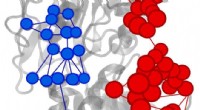 Kemikere finder et nyt værktøj til at forstå enzymer – GoogleEffektorudløst stigning (rød) eller reduktion (blå) af informationsstrømmen i IGPS-enzym. Kredit:Uriel Morzan Yale-forskere har taget en ny tilgang til at optrevle den komplekse struktur og regule
Kemikere finder et nyt værktøj til at forstå enzymer – GoogleEffektorudløst stigning (rød) eller reduktion (blå) af informationsstrømmen i IGPS-enzym. Kredit:Uriel Morzan Yale-forskere har taget en ny tilgang til at optrevle den komplekse struktur og regule
- Hvad gør Atomic Radius i en periode?
- Varmere og vådere klimaer forstærker kulstoffrigivelsen
- Majs med et låg af græs:Find den bedste kombination til majs med biobrændstof, jordbeskyttelse
- Hvilket grundstof bruges i atomkraftværker?
- Hvor mange elektroner skal svovl være en stabil oktet?
- Hvor dybt vil Providence Canyon være i 2050?


