Elektronegativitet og bindingstype:Forståelse af ioniske vs. kovalente bindinger
1. Elektronegativitet:Et mål for et atoms tiltrækning af elektroner
Elektronegativitet er en egenskab ved et atom, der beskriver dets tendens til at tiltrække elektroner mod sig selv, når det danner en kemisk binding. Jo højere elektronegativitetsværdien af et atom er, jo stærkere er dets tiltrækning på delte elektroner.
2. Forskellen i elektronegativitet dikterer bindingstype:
* Ionbindinger: Når forskellen i elektronegativitet mellem to atomer er stor (typisk større end 1,7), vil et atom have et meget stærkere træk på de delte elektroner. Dette fører til fuldstændig overførsel af elektroner fra det mindre elektronegative atom til det mere elektronegative atom, hvilket resulterer i dannelsen af ioner (positivt ladet kation og negativt ladet anion). Disse modsat ladede ioner holdes derefter sammen af elektrostatiske kræfter og danner en ionbinding.
* Kovalente bindinger: Når elektronegativitetsforskellen er lille (typisk mindre end 1,7), har ingen af atomerne et væsentligt stærkere træk på elektronerne. Dette resulterer i deling af elektroner mellem atomerne og danner en kovalent binding.
* Ikke-polære kovalente bindinger: Hvis elektronegativitetsforskellen er meget lille eller nul (som i en binding mellem to identiske atomer), deles elektronerne ligeligt mellem atomerne.
* Polære kovalente bindinger: Hvis elektronegativitetsforskellen er moderat, deles elektronerne ulige, hvilket skaber en delvis positiv ladning (δ+) på det mindre elektronegative atom og en delvis negativ ladning (δ-) på det mere elektronegative atom. Denne ujævne deling fører til en polær kovalent binding.
Opsummering:
* Stor elektronegativitetsforskel =Ionbinding
* Lille elektronegativitetsforskel =Kovalent binding (kan være upolær eller polær)
Eksempel:
* NaCl (natriumchlorid): Natrium (Na) har en elektronegativitet på 0,93, mens klor (Cl) har en elektronegativitet på 3,16. Forskellen er stor (2,23), hvilket resulterer i dannelsen af en ionbinding, hvor natrium mister en elektron for at blive en kation (Na+), og klor får en elektron til at blive en anion (Cl-).
* H2O (vand): Ilt (O) har en elektronegativitet på 3,44, mens brint (H) har en elektronegativitet på 2,20. Forskellen er moderat (1,24), hvilket fører til en polær kovalent binding, hvor oxygen har en delvis negativ ladning og brint har en delvis positiv ladning.
Husk, at elektronegativitet er et nyttigt værktøj til at forudsige bindingskarakter, men det er ikke den eneste faktor. Andre faktorer som atomstørrelse og antallet af elektronskaller kan også påvirke bindingstypen.
Sidste artikelForståelse af molekylenotation:Hvorfor fed skrift?
Næste artikelCæsium:Det mest reaktive metal - Forståelse af reaktivitet
 Varme artikler
Varme artikler
-
 Konstruerede mikrober kan producere bionedbrydeligt plast til lavere omkostninger og miljøpåvirkni…Langt størstedelen af plastik er lavet af fossile brændstoffer, og nedbrydes ikke biologisk. Plastforurening hober sig op i vores have og vandveje, og mikroplast kommer i jorden, dyr, og endda vores
Konstruerede mikrober kan producere bionedbrydeligt plast til lavere omkostninger og miljøpåvirkni…Langt størstedelen af plastik er lavet af fossile brændstoffer, og nedbrydes ikke biologisk. Plastforurening hober sig op i vores have og vandveje, og mikroplast kommer i jorden, dyr, og endda vores -
 Verdens mindste sensor måler planters vækstkraft, dyr og menneskerKredit:Wageningen University &Research Hvordan visualiserer du de ekstremt små kræfter, der er forbundet med processer såsom embryonal vækst og udvikling? Forskere ved Wageningen har eksperimenter
Verdens mindste sensor måler planters vækstkraft, dyr og menneskerKredit:Wageningen University &Research Hvordan visualiserer du de ekstremt små kræfter, der er forbundet med processer såsom embryonal vækst og udvikling? Forskere ved Wageningen har eksperimenter -
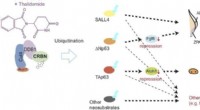 Molekylær basis for lægemiddelvirkninger på lemmer og øreudvikling afsløretThalidomid binder sig til cereblon (CRBN) og forårsager unormal lem- og øreudvikling ved at fremkalde nedbrydning af proteiner kaldet? Np63α og TAp63α gennem en proces kendt som ubiquitination. Denne
Molekylær basis for lægemiddelvirkninger på lemmer og øreudvikling afsløretThalidomid binder sig til cereblon (CRBN) og forårsager unormal lem- og øreudvikling ved at fremkalde nedbrydning af proteiner kaldet? Np63α og TAp63α gennem en proces kendt som ubiquitination. Denne -
 DIY Ballon Flydende:Sådan løfter du balloner uden heliumAf Claire Gillespie Opdateret 24. marts 2022 twpixels/iStock/GettyImages En luftballon kan se meget anderledes ud end en heliumballon, men princippet bag, hvordan de to typer balloner fungerer, er
DIY Ballon Flydende:Sådan løfter du balloner uden heliumAf Claire Gillespie Opdateret 24. marts 2022 twpixels/iStock/GettyImages En luftballon kan se meget anderledes ud end en heliumballon, men princippet bag, hvordan de to typer balloner fungerer, er
- Klorofyl:Nøgleplantemolekylet for energiabsorption
- Hvad er genetisk materiale indeholdt i et individ?
- Hvad gør atomerne under en reaktion, der viser, at de overholder bevarelse af masse?
- Hvad er smeltepunktet for C6H12O6?
- Hvor meget energi har en X-stråle med 8 nm (810-9m) bølgelængde)?
- Undersøgelse afslører fordomme stærkt påvirket af ulighed


