Methyl Orange Titrering:Mekanisme i syre-base kemi (Na2CO3 &HCl)
1. Kemien af Methyl Orange
* Methylappelsin er en svag syre, der findes i to former:
* Syreform (HIn): Rød farve
* Basisform (In-): Gul farve
* Ligevægten mellem disse former er beskrevet ved følgende ligning:
HIn (rød) ⇌ H+ + In- (gul)
* Placeringen af denne ligevægt påvirkes af opløsningens pH.
2. Titreringsproces
* Udgangstilstand: Ved begyndelsen af titreringen indeholder opløsningen natriumcarbonat (Na2CO3), en svag base. Dette skaber et lidt basalt miljø. Methylorange, som er en svag syre, er for det meste i sin baseform (In-), hvilket resulterer i en gul løsning.
* Som HCl tilføjes: Når du tilsætter saltsyre (HCl), reagerer det med natriumcarbonatet. Denne reaktion forbruger hydroxidioner (OH-), hvilket flytter ligevægten mod den sure side. Dette får mere af methylorangen til at gå fra baseformen (In-) til syreformen (HIn).
* Ækvivalenspunkt: Ækvivalenspunktet nås, når de tilsatte mol HCl er lig med de tilstedeværende mol Na2CO3. På dette tidspunkt er opløsningen overvejende sammensat af den svage syre H2CO3 (kulsyre). Opløsningens pH er omkring 4,5, hvilket er det første ækvivalenspunkt for titreringen.
* Slutpunkt: slutpunktet af titreringen sker, når indikatoren skifter farve. I dette tilfælde ændres methylorange fra gul til orange (en blanding af rød og gul). Denne farveændring sker, når pH-værdien af opløsningen når methylorangens pH-område (3,1-4,4).
* Andet ækvivalenspunkt: Yderligere tilsætning af HCl fører til det andet ækvivalenspunkt, hvor alle carbonationerne neutraliseres. På dette tidspunkt er opløsningen overvejende sammensat af den svage syre H2CO3 og dens konjugerede base HCO3-. Opløsningens pH er omkring 8,3.
3. Hvorfor Methyl Orange er velegnet
Methylorange er en passende indikator for denne titrering, fordi:
* Klar farveændring: Farveændringen fra gul til orange er tydelig og let synlig.
* pH-område: pH-området for methylorange (3,1-4,4) overlapper med titreringens første ækvivalenspunkt (pH ~ 4,5). Dette sikrer, at indikatoren skifter farve tæt på det punkt, hvor al Na2CO3 har reageret med HCl.
Opsummering: Methyloranges farveændring under titreringen af natriumcarbonat med saltsyre afspejler ændringen i pH, da den stærke syre neutraliserer den svage base. Farveændringen signalerer slutpunktet for titreringen, som er tæt på reaktionens første ækvivalenspunkt.
Sidste artikelRedox-halvreaktioner:Forståelse af elektronoverførsel
Næste artikelMethyl Orange som titreringsindikator:Funktion og betydning
 Varme artikler
Varme artikler
-
 Sikker syrefortynding:Derfor skal du tilføje syre til vand, ikke omvendtIvanMikhaylov/iStock/GettyImages Hvorfor fortynde syrer? Fortynding af en syre reducerer den samlede mængde af opløst stof i opløsningen. Det svækker ikke syrens kemiske reaktivitet; det sænker simpe
Sikker syrefortynding:Derfor skal du tilføje syre til vand, ikke omvendtIvanMikhaylov/iStock/GettyImages Hvorfor fortynde syrer? Fortynding af en syre reducerer den samlede mængde af opløst stof i opløsningen. Det svækker ikke syrens kemiske reaktivitet; det sænker simpe -
 Belyse spørgsmålet om vinsvindelKredit:University of Adelaide University of Adelaide vinforskere er ved at udvikle en hurtig og enkel metode til at autentificere vin - en potentiel løsning mod den anslåede vinsvindel for milliar
Belyse spørgsmålet om vinsvindelKredit:University of Adelaide University of Adelaide vinforskere er ved at udvikle en hurtig og enkel metode til at autentificere vin - en potentiel løsning mod den anslåede vinsvindel for milliar -
 En ny ligand forlænger halveringstiden for peptider fra minutter til dageEt bicyklisk peptid (hvidt) bundet til serumalbumin (rødt) gennem den nyudviklede ligand (grøn), flyder i blodbanen. Kredit:C. Heinis/EPFL EPFL-forskere har udviklet et ligandmolekyle, der forbind
En ny ligand forlænger halveringstiden for peptider fra minutter til dageEt bicyklisk peptid (hvidt) bundet til serumalbumin (rødt) gennem den nyudviklede ligand (grøn), flyder i blodbanen. Kredit:C. Heinis/EPFL EPFL-forskere har udviklet et ligandmolekyle, der forbind -
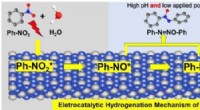 Hydrogeneringsregulering af nitrobenzen i elektrokatalytiske processer realiseretGrafisk abstrakt. En omfattende forståelse af selektiviteten over for elektrokatalytiske hydrogeneringsprodukter af nitrobenzen blev udført eksperimentelt og teoretisk over en Cu3Pt/C -legeringskataly
Hydrogeneringsregulering af nitrobenzen i elektrokatalytiske processer realiseretGrafisk abstrakt. En omfattende forståelse af selektiviteten over for elektrokatalytiske hydrogeneringsprodukter af nitrobenzen blev udført eksperimentelt og teoretisk over en Cu3Pt/C -legeringskataly
- Hvad udgør et kropssystem?
- Egenskaber af Natural & Synthetic Rubber
- Alle følgende er funktioner menneskelig hud undtagen?
- Samproduktion forbinder forskning og handling for bæredygtighed
- Identificer moderne bioteknologi fra traditionel bioteknologi?
- Er placeringerne af magnetisk sydpol og geografisk nord nær Antarktis eller Arctic?


