Redox-halvreaktioner:Forståelse af elektronoverførsel
Redox Half Reactions:The Story of Electron Transfer
Redoxreaktioner involverer overførsel af elektroner mellem kemiske arter. I stedet for at se på hele reaktionen kan vi dele den op i to halvreaktioner , der hver repræsenterer oxidations- eller reduktionsprocessen, der foregår separat.
1. Oxidationshalvreaktion:
- Denne halvreaktion viser tabet af elektroner af en art.
- Arten, der gennemgår oxidation, kaldes reduktionsmidlet (det forårsager reduktion i en anden art).
- Elektroner vises som produkter i højre side af ligningen.
Eksempel:
Fe2+(vandig) → Fe3+(vandig) + e⁻
(Jern(II) mister en elektron og bliver til jern(III))
2. Reduktion af halvreaktion:
- Denne halvreaktion viser gevinsten af elektroner af en art.
- Arten, der gennemgår reduktion, kaldes oxidationsmidlet (det forårsager oxidation i en anden art).
- Elektroner optræder som reaktanter i venstre side af ligningen.
Eksempel:
Cu²⁺(aq) + 2e⁻ → Cu(s)
(Kobber(II) får to elektroner til at blive til fast kobber)
Nøglepunkter:
- Balancering: Begge halvreaktioner skal afbalanceres med hensyn til atomer og ladning. Dette involverer ofte tilsætning af vand (H2O), hydrogenioner (H⁺) eller hydroxidioner (OH⁻) afhængigt af reaktionens miljø (surt, basisk eller neutralt).
- Kombinering: De to halvreaktioner kan kombineres for at danne den overordnede afbalancerede redoxreaktion. Dette indebærer justering af koefficienter for at sikre, at antallet af elektroner tabt ved oxidation svarer til antallet af elektroner opnået ved reduktion.
Hvorfor er halvreaktioner nyttige?
- Forenkling af komplekse reaktioner: De gør det lettere at forstå elektronoverførselsprocessen.
- Forudsigelse af reaktionsgennemførlighed: De hjælper med at afgøre, om en reaktion vil opstå spontant eller ej.
- Forståelse af elektrokemiske celler: De er vigtige for at beskrive batteriernes og brændselscellernes funktion.
Eksempel på at kombinere halvreaktioner:
Lad os kombinere oxidations- og reduktionshalvreaktionerne fra eksemplerne ovenfor:
Oxidation: Fe2+(vandig) → Fe3+(vandig) + e⁻
Reduktion: Cu²⁺(aq) + 2e⁻ → Cu(s)
Sådan kombinerer du dem:
1. Gang oxidationshalvreaktionen med 2 for at balancere elektronerne:2Fe²⁺(aq) → 2Fe³⁺(aq) + 2e⁻
2. Læg de to halvreaktioner sammen:2Fe²⁺(aq) + Cu²⁺(aq) + 2e⁻ → 2Fe³⁺(aq) + Cu(s) + 2e⁻
3. Annuller elektronerne:2Fe²⁺(aq) + Cu²⁺(aq) → 2Fe³⁺(aq) + Cu(s)
Dette er den overordnede afbalancerede redoxreaktion.
At forstå redox-halvreaktioner er afgørende for at forstå og analysere en lang række kemiske processer. Ved at nedbryde redoxreaktioner i disse enklere trin får vi værdifuld indsigt i deres mekanismer og potentielle anvendelser.
 Varme artikler
Varme artikler
-
 Nye måder at lave plantebaseret medicin på i rummet og på jordenKredit:CC0 Public Domain Hvordan kan man lave medicin i rummet? Det er et svært spørgsmål, da mange lægemidler, vi nyder på Jorden, bruger kemikalier, der kommer fra planter, og pladsen er næsten
Nye måder at lave plantebaseret medicin på i rummet og på jordenKredit:CC0 Public Domain Hvordan kan man lave medicin i rummet? Det er et svært spørgsmål, da mange lægemidler, vi nyder på Jorden, bruger kemikalier, der kommer fra planter, og pladsen er næsten -
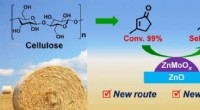 Forskere syntetiserer bio-baseret methylcyclopentadien med 3-methylcyclopent-2-enonDirekte hydrodeoxygenering af MCP til MCPD på den delvist reducerede Zn-Mo-oxidkatalysator. Kredit:DICP Methylcyclopentadien (MCPD) er en vigtig monomer i produktionen af RJ-4 brændstof, et rake
Forskere syntetiserer bio-baseret methylcyclopentadien med 3-methylcyclopent-2-enonDirekte hydrodeoxygenering af MCP til MCPD på den delvist reducerede Zn-Mo-oxidkatalysator. Kredit:DICP Methylcyclopentadien (MCPD) er en vigtig monomer i produktionen af RJ-4 brændstof, et rake -
 Fryseramme:Forskere løser, hvordan celler folder proteiner udKredit:CC0 Public Domain En glad celle er en balanceret celle, men for hvert fantastisk snoet protein, det skaber, den skal rive de gamle i stykker. Det betyder at udrede en indviklet kringleligne
Fryseramme:Forskere løser, hvordan celler folder proteiner udKredit:CC0 Public Domain En glad celle er en balanceret celle, men for hvert fantastisk snoet protein, det skaber, den skal rive de gamle i stykker. Det betyder at udrede en indviklet kringleligne -
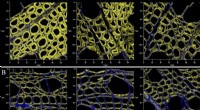 Kvantificering af ændringer i overfladekemi af træplanter under mikrobiel gæringORNL -forskere brugte sofistikerede laserscanningsteknikker til at sammenligne nedbrydningen af fermenteret populær (B) sammenlignet med ugæret populær (A), som de kvantificerede, for første gang, k
Kvantificering af ændringer i overfladekemi af træplanter under mikrobiel gæringORNL -forskere brugte sofistikerede laserscanningsteknikker til at sammenligne nedbrydningen af fermenteret populær (B) sammenlignet med ugæret populær (A), som de kvantificerede, for første gang, k
- Hvilke overgange er mulige i henhold til klippecyklussen?
- Californiske agenturer er uenige om Colorado River tørkeplan
- Hvilken form for naturlig udvælgelse er mest sandsynligt at spille en rolle i speciation?
- Hvorfor betragtes generalbiologi som et vigtigt emne på det kursus, du tager?
- IMERG tilføjer kraftig nedbør fra Tropical Storm Damrey
- Hvordan indfødte folk i Amazonas håndterer coronavirus-pandemien


