Forstå buffere og hydroxidioner:hvordan de interagerer
Her er hvorfor:
* Buffere modstår ændringer i pH. Det er opløsninger, der kan neutralisere små mængder tilsat syre eller base uden væsentlige ændringer i pH.
* Hydroxidioner er basiske. Tilføjelse af et stort antal hydroxidioner til en opløsning vil gøre den mere basisk (øge pH).
* For at danne en buffer skal du bruge en svag syre og dens konjugerede base (eller en svag base og dens konjugerede syre). Disse par kan neutralisere både tilsat syre og base.
Tænk på det sådan her:
* At tilføje hydroxidioner er som at tilføje base til en opløsning. Det vil øge pH.
* En buffer kræver både sure og basiske komponenter for at være effektiv. Tilsætning af kun hydroxidioner vil gøre opløsningen mere basisk, ikke skabe en buffer.
Eksempel:
Du ville ikke skabe en buffer ved blot at tilføje en stor mængde NaOH (som frigiver hydroxidioner) til vand. Dette ville blot være en stærk grundlæggende løsning.
For at skabe en buffer skal du tilføje en svag syre (som eddikesyre) og dens konjugerede base (acetationer).
Sidste artikelIdentifikation af kilderne til svovloxider (SOx)
Næste artikelOpløsende kulstof:kemiske reaktioner og syrer forklaret
 Varme artikler
Varme artikler
-
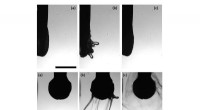 Polymerer forhindrer potentielt farlig tåge under tandlægebesøgBrug af polyakrylsyreopløsning i vand som vandingsvæske i tandplejen reducerer risikoen for aerosolformede patogener. Her, polymeren er vist og danner slangelignende tråde nær spidsen af en vibreren
Polymerer forhindrer potentielt farlig tåge under tandlægebesøgBrug af polyakrylsyreopløsning i vand som vandingsvæske i tandplejen reducerer risikoen for aerosolformede patogener. Her, polymeren er vist og danner slangelignende tråde nær spidsen af en vibreren -
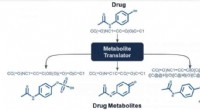 Dyb læring giver lægemiddeldesign et løftEt beregningsværktøj skabt på Rice University kan hjælpe medicinalvirksomheder med at udvide deres evne til at undersøge lægemidlers sikkerhed. Kredit:Kavraki Lab/Rice University Når du tager medi
Dyb læring giver lægemiddeldesign et løftEt beregningsværktøj skabt på Rice University kan hjælpe medicinalvirksomheder med at udvide deres evne til at undersøge lægemidlers sikkerhed. Kredit:Kavraki Lab/Rice University Når du tager medi -
 At gå atomkraft på månen og MarsKredit:CC0 Public Domain Det lyder måske som science fiction, men videnskabsmænd forbereder sig på at bygge kolonier på månen og, til sidst, Mars. Med NASA planlægning af sin næste menneskelige mi
At gå atomkraft på månen og MarsKredit:CC0 Public Domain Det lyder måske som science fiction, men videnskabsmænd forbereder sig på at bygge kolonier på månen og, til sidst, Mars. Med NASA planlægning af sin næste menneskelige mi -
 Forskere demonstrerer fundamentalt ny tilgang til ultralydsbilleddannelseKredit:CC0 Public Domain Forskere fra North Carolina State University har demonstreret en ny teknik til at lave ultralydsbilleder. Den nye tilgang er væsentligt enklere end eksisterende teknikker
Forskere demonstrerer fundamentalt ny tilgang til ultralydsbilleddannelseKredit:CC0 Public Domain Forskere fra North Carolina State University har demonstreret en ny teknik til at lave ultralydsbilleder. Den nye tilgang er væsentligt enklere end eksisterende teknikker
- Arkæologer reviderer kronologien for de sidste jæger-samlere i Mellemøsten
- Video:Flyver under Aeolus
- Ny analyse afslører udfordringer for tørkehåndtering i Oregons Willamette River Basin
- Hvorfor bruger vi bare den vedvarende energi i stedet?
- Sådan fungerer ting:Socialt netværk
- Hvad er adapter i rekombinant DNA -teknologi?


