Kaliumnitratreaktionseksperimenter:sikkerhed, procedurer og anvendelser
Kittisak Kaewchalun / Getty Images
Kaliumnitrat (KNO3 ) er et ionisk salt sammensat af kaliumioner (K + ) og nitrationer (NO3). - ). Det er meget udbredt i laboratoriemiljøer på grund af dets stærke oxiderende egenskaber og dets evne til at reagere med en række organiske og uorganiske forbindelser.
TL;DR (for lang; læste ikke)
Du kan roligt udforske kaliumnitratreaktioner med sukker, syrer og svovl under korrekt opsyn. Eksperimenterne involverer håndtering af koncentrerede syrer og giftige dampe, så et velventileret laboratorium, PPE og strenge sikkerhedsprotokoller er obligatoriske.
Kaliumnitrat og sukker
Kaliumnitrat fungerer som et fremragende oxidationsmiddel, der leverer ilt til hurtig forbrænding. Når en lille mængde KNO3 blandes med spisesukker (saccharose) og antændes på en ikke-brændbar overflade, brænder sukkeret kraftigt og producerer kuldioxid, vanddamp og et varmeudbrud. Denne reaktion er kernekemien bag den 4. juli stjernekastere, hvor KNO3 , sukker og metalspåner kombineres for at generere skarpt lys. Det er også den grundlæggende reaktion i sukker-raketbrændstof, hvor varmen driver de gasser, der driver raketten frem. Udfør kun denne demonstration i et overvåget laboratoriemiljø, iført briller, handsker og en laboratoriefrakke, og brug en ildslukker og et stinkskab.
Kaliumnitrat og svovlsyre
Blanding af koncentreret svovlsyre (H2 SO4 ) med tør KNO3 giver salpetersyre (HNO3 Efter opvarmning af blandingen for at inducere destillation. Reaktionen frigiver ætsende og giftige dampe, hvilket gør den uegnet til amatørkemikere. Denne protokol bør kun udføres i et velventileret laboratorium med passende PPE og syrebestandigt udstyr.
Kaliumnitrat, svovl og trækul (krudt)
Den klassiske formulering af sort pulver – 75 % kaliumnitrat, 15 % trækul og 10 % svovl – er afhængig af den oxiderende kraft af KNO3 og svovls og trækuls brændbare natur. Form ingredienserne til en fin konsistens, og opløs derefter KNO3 i vand og opvarm for at fordampe opløsningen. Tilsæt trækul og svovl, omrør isopropylalkohol, afkøl, filtrer og tør blandingen. Sigt det tørrede pulver for at opnå ensartet partikelstørrelse. Denne blanding producerer en hurtig gasfrigivelse med stort volumen, når den antændes. På grund af det eksplosive potentiale kræver dette eksperiment strenge sikkerhedsprotokoller, herunder et eksplosionsskjold, stinkskab og overvåget håndtering.
Referencer
 Varme artikler
Varme artikler
-
 Løsning af strukturen af ATP -syntaseStruktur af den monomere gær -ATP -syntase, vist som en overfladerepræsentation, som bestemt ved kryo-elektronmikroskopi. Kredit:Rosalind Franklin University Et team af forskere ledet af Rosalind
Løsning af strukturen af ATP -syntaseStruktur af den monomere gær -ATP -syntase, vist som en overfladerepræsentation, som bestemt ved kryo-elektronmikroskopi. Kredit:Rosalind Franklin University Et team af forskere ledet af Rosalind -
 Nye værktøjer til at karakterisere biofilms fysiske egenskaberFigur (a) og (b) viser fluorescens- og oxygenkoncentrationskortet for henholdsvis en bakteriemikrokoloni. Figur (c) viser linjeprofilen af fluorescens (cirkler) og oxygenkoncentration (trekanter) la
Nye værktøjer til at karakterisere biofilms fysiske egenskaberFigur (a) og (b) viser fluorescens- og oxygenkoncentrationskortet for henholdsvis en bakteriemikrokoloni. Figur (c) viser linjeprofilen af fluorescens (cirkler) og oxygenkoncentration (trekanter) la -
 Genbrug af 1 kg tøj sparer 25 kg CO2, viser undersøgelseEn stigning på 10 % i brugtsalg kan spare 3 % af CO2-udledningen og 4 % af vandet. Kredit:Moda re- (Cáritas) UPCs INTEXTER har foretaget en analyse for at beregne andelen af fibre, der bruges i d
Genbrug af 1 kg tøj sparer 25 kg CO2, viser undersøgelseEn stigning på 10 % i brugtsalg kan spare 3 % af CO2-udledningen og 4 % af vandet. Kredit:Moda re- (Cáritas) UPCs INTEXTER har foretaget en analyse for at beregne andelen af fibre, der bruges i d -
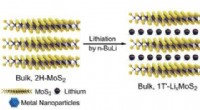 Brintproduktion i et begrænset rumFigur 1:Indkapslingen af ædelmetal nanopartikler i MoS2 ved en in-situ reduktion strategi. National University of Singapore kemikere har udviklet en metode til at begrænse ædelmetal -nanopartikl
Brintproduktion i et begrænset rumFigur 1:Indkapslingen af ædelmetal nanopartikler i MoS2 ved en in-situ reduktion strategi. National University of Singapore kemikere har udviklet en metode til at begrænse ædelmetal -nanopartikl
- Affaldsøer ud for Mellemamerika indikerer havforureningsproblem
- Sådan fungerer Earth 911.org
- Forskere isolerer kræftstamceller ved hjælp af en ny metode
- Hvilken himmelsk krop kan ses som en lys stjerne i den østlige himmel ved daggry?
- Hvilken gruppe er tæt knyttet til Archeabacteria?
- Nanoblaster fra laseraktiverede nanopartikler flytter molekyler, proteiner og DNA ind i cellerne


