Beregning af isoleret udbytte i kemiske reaktioner
Af Robert Schrader – Opdateret 30. august 2022
I kemi, udbytte kvantificerer mængden af produkt produceret i en reaktion. To hovedudbytter tages i betragtning:det teoretiske udbytte, som er den maksimale mængde forudsagt af støkiometri, og det faktiske eller isolerede udbytte, som er mængden af produkt, du genvinder fra reaktionsbeholderen. Sammenligning af det isolerede udbytte med det teoretiske udbytte giver procentudbyttet, en nøglemåling til evaluering af reaktionseffektivitet.
Trin 1 – Balancer ligningen
Før enhver beregning skal du afbalancere reaktionen for at sikre, at antallet af atomer i hvert grundstof er det samme på begge sider. For eksempel kan nedbrydningen af kobber(II)nitrat, Cu(NO₃)₂, skrives som:
2Cu(NO₃)₂→2CuO+4NO₂+O₂
I denne afbalancerede ligning optræder hvert element i samme mængde på reaktant- og produktsiden.
Trin 2 – Bestem molære masser
Beregn molmasserne af de relevante faste stoffer. For Cu(NO3)2 er den molære masse 187,56 gmol-1; for CuO er det 79,55 gmol⁻¹. Gasser udelades fra udbytteberegningen, fordi de ikke bidrager til den isolerede masse.
Trin 3 – Konverter startmasse til mol
Hvis du begynder med 250,04 g Cu(NO₃)₂, er antallet af mol:
250,04 g ÷ 187,56 gmol⁻¹=1,33mol
Trin 4 – Beregn teoretisk udbytte
Fra den afbalancerede ligning producerer 2mol Cu(NO₃)₂ 2mol CuO. Således skulle 1,33 mol Cu(NO₃)₂ give 1,33 mol CuO, svarende til:
1,33 mol × 79,55 gmol⁻¹=105,80 g CuO (teoretisk udbytte)
Trin 5 – Mål faktisk udbytte og beregn procentudbytte
Antag, at eksperimentet giver 63,41 g CuO. Det procentvise udbytte beregnes som:
63,41 g ÷ 105,80 g=0,5993→59,93 %
Nødvendige materialer
- Periodisk tabel over elementerne
- Videnskabelig lommeregner
- Reagenser og reaktionsapparater
- Elektronisk balance
TL;DR
For at beregne isoleret udbytte skal du først afbalancere reaktionen, derefter bestemme molmasser, omregne startmassen til mol, beregne det teoretiske udbytte ud fra støkiometri og til sidst sammenligne den målte masse af produktet med den teoretiske masse for at opnå det procentvise udbytte.
 Varme artikler
Varme artikler
-
 Proteinernæring til celler og organismer:Kan vi bruge det til behandling af sygdomme?Bindingsstedet for EAAT1-hæmmeren (UCPH101) opløses ved røntgenkrystallografi og er placeret i en afstand fra substratbindingsstedet. Substratet er vist i midten af transportøren, mens inhibitoren e
Proteinernæring til celler og organismer:Kan vi bruge det til behandling af sygdomme?Bindingsstedet for EAAT1-hæmmeren (UCPH101) opløses ved røntgenkrystallografi og er placeret i en afstand fra substratbindingsstedet. Substratet er vist i midten af transportøren, mens inhibitoren e -
 Se gennem jord kan hjælpe landmændene med at håndtere fremtidige tørkeperioderPrinceton-forskere brugte borosilikatglasperler som erstatning for jord til at studere adfærden af hydrogeler, der fungerer som vandreservoirer på landbrugsmarker. Forskerne brugte et tilsætningssto
Se gennem jord kan hjælpe landmændene med at håndtere fremtidige tørkeperioderPrinceton-forskere brugte borosilikatglasperler som erstatning for jord til at studere adfærden af hydrogeler, der fungerer som vandreservoirer på landbrugsmarker. Forskerne brugte et tilsætningssto -
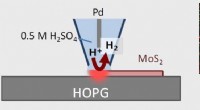 Billedbehandlingsteknik giver katalytisk 2-D materialeteknik et bedre udsynScanning elektrokemisk cellemikroskopi (SECCM) muliggør billeddannelse og kvantitativ analyse af hydrogenudviklingsreaktion (HER) katalytisk aktive steder i 1H MoS 2 monolag. Kredit:Kanazawa Univers
Billedbehandlingsteknik giver katalytisk 2-D materialeteknik et bedre udsynScanning elektrokemisk cellemikroskopi (SECCM) muliggør billeddannelse og kvantitativ analyse af hydrogenudviklingsreaktion (HER) katalytisk aktive steder i 1H MoS 2 monolag. Kredit:Kanazawa Univers -
 En termisk isoleringskomposit af hule silicapartikler blandet med cellulosefibreORNL-forskere lavede en termisk isoleringskomposit af hule silicapartikler ved at blande partiklerne med cellulosefibre. Kompositten viste sig at være meget fugtstabil og udviser potentiale for anvend
En termisk isoleringskomposit af hule silicapartikler blandet med cellulosefibreORNL-forskere lavede en termisk isoleringskomposit af hule silicapartikler ved at blande partiklerne med cellulosefibre. Kompositten viste sig at være meget fugtstabil og udviser potentiale for anvend
- Hvad er de globale mønstre for jordskælv?
- Er Apollo himmelens Gud?
- Hvad er et plateau, der ligger ved hver kyst på kontinentet?
- Hvordan kan de biotiske faktorer i et økosystem påvirke abiotiske faktorer?
- Fattigdom forværrede 2020, da mange lavtlønsarbejdere tog hovedparten af de økonomiske slag
- Philly start-up Kapsul laver et mere støjsvagt klimaanlæg takket være $2,3 millioner fra crowdfun…


