Forståelse af Gibbs Free Energy:Forudsigelse af kemisk reaktionsretning
Af Andrea Becker | Opdateret 30. august 2022
michaeljung/iStock/Getty Images
I de fleste indledende kemikurser er reaktioner vist med en enkelt pil, hvilket indebærer en envejsproces. I virkeligheden er kemiske reaktioner reversible, og den retning, de favoriserer, afhænger af systemets Gibbs frie energi (ΔG). Ved at evaluere ΔG kan videnskabsmænd forudsige, om en reaktion vil fortsætte fremad, tilbage eller nå ligevægt.
Entalpi (ΔH)
Entalpi repræsenterer den samlede energi, der er lagret i et system, hovedsageligt hidrørende fra molekylernes tilfældige bevægelse. Det er ikke det samme som potentiel energi af bindinger eller kinetisk energi af bulk bevægelse. Entalpi ændres, når varme eller arbejde tilføres eller fjernes, og den påvirkes af tryk og volumen - især i gasser.
Entropi (ΔS)
Entropi måler graden af uorden eller tilfældighed i et system. Når et system mister varme, såsom vand, der fryser til is, falder dets entropi, fordi molekylerne vedtager et mere ordnet arrangement. På den universelle skala aftager entropien aldrig; det har altid en tendens til at stige.
Temperaturens rolle
Både entalpi og entropi er temperaturafhængige. Tilførsel af varme hæver både ΔH og ΔS. Gibbs frie energiændring beregnes som ΔG =ΔH – TΔS, hvor T er den absolutte temperatur i Kelvin. Fordi temperatur multiplicerer entropi-leddet, kan den vippe balancen mellem entalpi og entropi, hvilket ændrer reaktionens spontanitet.
Konsekvenser for kemiske reaktioner
Ved at undersøge ΔG kan kemikere bestemme reaktionsgennemførlighed:
- ΔG < 0 – reaktionen er spontan og fortsætter i fremadgående retning.
- ΔG > 0 – reaktionen er ikke-spontan og har tendens til at vende.
- ΔG = 0 – systemet er i ligevægt; frem og tilbage kurser er ens.
Når entalpi og entropi favoriserer modsatte retninger, bliver temperaturen den afgørende faktor. For eksempel kan en endoterm reaktion (ΔH > 0) med positiv ΔS blive spontan ved høje temperaturer, fordi TΔS-udtrykket opvejer ΔH.
At forstå Gibbs frie energi ruster forskere til at designe effektive processer, forudsige reaktionsveje og kontrollere industriel syntese.
Sidste artikelMestring af satslove:En trin-for-trin-vejledning for kemikere
Næste artikelBeregning af isoleret udbytte i kemiske reaktioner
 Varme artikler
Varme artikler
-
 Østersskaller inspirerer til ny metode til at gøre superstærke, fleksible polymererEn figur, der illustrerer, at polymerkrystallisationshastighed kan bruges til at kontrollere den rumlige fordeling af nanopartikler. Urenheder (her, nanopartiklerne) vil blive opslugt af krystallen, h
Østersskaller inspirerer til ny metode til at gøre superstærke, fleksible polymererEn figur, der illustrerer, at polymerkrystallisationshastighed kan bruges til at kontrollere den rumlige fordeling af nanopartikler. Urenheder (her, nanopartiklerne) vil blive opslugt af krystallen, h -
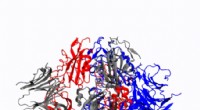 Kemiker udvikler 3D-simuleringer af proteiner til spike i coronavirusAnimation, der viser, hvordan coronavirus -spike -protein ændrer form lige før det bindes til human celleceptor. Kredit:Illustration leveret af Mahmoud Moradi. Beregningskemiker Mahmoud Moradi vil
Kemiker udvikler 3D-simuleringer af proteiner til spike i coronavirusAnimation, der viser, hvordan coronavirus -spike -protein ændrer form lige før det bindes til human celleceptor. Kredit:Illustration leveret af Mahmoud Moradi. Beregningskemiker Mahmoud Moradi vil -
 3D-ordnet kanal forbedrer elektrokatalyseGrafisk abstrakt. Kredit:DOI:10.1021/jacs.1c04653 Et team ledet af prof. YU Shuhong og prof. HOU Zhonghuai fra University of Science and Technology of China (USTC) fra det kinesiske videnskabsakad
3D-ordnet kanal forbedrer elektrokatalyseGrafisk abstrakt. Kredit:DOI:10.1021/jacs.1c04653 Et team ledet af prof. YU Shuhong og prof. HOU Zhonghuai fra University of Science and Technology of China (USTC) fra det kinesiske videnskabsakad -
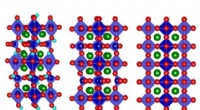 Elektrisk varmeventil:Strontium cobaltoxid tynd film ændrer termiske egenskaber med påført spænd…Forskere fandt ud af, at selen cobaltoxid (SCO) naturligt forekommer i en atomart konfiguration kaldet brownmillerite (midten), men når oxygenioner tilsættes (til højre), det bliver mere velordnet og
Elektrisk varmeventil:Strontium cobaltoxid tynd film ændrer termiske egenskaber med påført spænd…Forskere fandt ud af, at selen cobaltoxid (SCO) naturligt forekommer i en atomart konfiguration kaldet brownmillerite (midten), men når oxygenioner tilsættes (til højre), det bliver mere velordnet og
- Sådan rengøres vand
- I en fotocellelysenergi omdannes til?
- Hvor lang tid tager det for Jorden at gennemføre en fuld bane rundt om solen, også kendt som et pl…
- Hvordan man lærer matematik til ADHD Children
- Internetfirmaet begrænser registreringer af websteder med virustema
- Hvilke energitransformationer forekommer i en brand?


