Sådan løses en neutraliseringsreaktion:Trin-for-trin-vejledning
Af Mara Pesacreta Opdateret 30. august 2022
En neutraliseringsreaktion opstår, når en stærk syre reagerer med en stærk base, hvilket giver vand og et salt. At beherske disse ligninger er afgørende for laboratoriearbejde og for at forstå de grundlæggende skel mellem syrer og baser. Referencetabeller over almindelige stærke syrer og baser leveres rutinemæssigt.
Trin 1
Identificer reaktanterne og skriv deres kemiske formler. Problemformuleringen vil specificere syre og base – for eksempel saltsyre (HCl) og natriumhydroxid (NaOH).
Trin 2
Bekræft, at den anførte syre faktisk er stærk og basen er stærk. Hvis det er uklart, se en standardtabel over stærke syrer og baser. I vores eksempel er HCl den stærke syre og NaOH den stærke base.
Trin 3
Identificer reaktionstypen. Neutralisering er en klassisk dobbeltforskydningsreaktion (syre-base):H⁺ fra syreparret med OH⁻ fra basen og danner vand, mens de resterende ioner kombineres og producerer saltet.
Trin 4
Skriv den ubalancerede ligning:HCl + NaOH → H₂O + NaCl.
Trin 5
Tjek balancen. I dette tilfælde er ligningen allerede afbalanceret:to H-atomer, et Cl, et Na og et O vises på hver side.
Ting påkrævet
- Periodisk tabel
- Computer
- Kemibog
- Pen
- Papir
Sidste artikelSubatomære partikler:byggestenene mindre end et atom
Næste artikelHvordan reaktantmasse påvirker kemiske reaktionshastigheder
 Varme artikler
Varme artikler
-
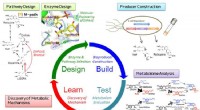 Konstruerede smarte celler forbedrer produktionen af farmaceutiske råvarerFigur 1 - Et design, Byg, Prøve, Lær workflow aktiveret forbedring af alkaloidproduktion. Kredit:Kobe University Forskere i Japan har udviklet et integreret syntetisk biologisk system til at konst
Konstruerede smarte celler forbedrer produktionen af farmaceutiske råvarerFigur 1 - Et design, Byg, Prøve, Lær workflow aktiveret forbedring af alkaloidproduktion. Kredit:Kobe University Forskere i Japan har udviklet et integreret syntetisk biologisk system til at konst -
 Elektrostatisk kontrollerede overfladegrænseforhold i nematiske flydende krystaller og kolloiderKarakterisering af blodpladernes størrelse og orientering i nematisk LC. SEM-mikrofotografier af blodplader før (A) og efter (B) SiO2-coating. (C) TEM mikroskop af partikler. Indsatsen viser SiO2-lage
Elektrostatisk kontrollerede overfladegrænseforhold i nematiske flydende krystaller og kolloiderKarakterisering af blodpladernes størrelse og orientering i nematisk LC. SEM-mikrofotografier af blodplader før (A) og efter (B) SiO2-coating. (C) TEM mikroskop af partikler. Indsatsen viser SiO2-lage -
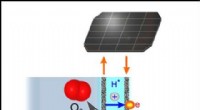 Forskerteamet fører an i et grønt kemi -gennembrud for vedvarende energiElektrolytisk vandopdeling:ilt- og brintudviklingsreaktioner finder sted ved anoden og katoden, som er adskilt af en sur protonledende elektrolyt. Kredit:Monash University Elektrolytisk vandopdeli
Forskerteamet fører an i et grønt kemi -gennembrud for vedvarende energiElektrolytisk vandopdeling:ilt- og brintudviklingsreaktioner finder sted ved anoden og katoden, som er adskilt af en sur protonledende elektrolyt. Kredit:Monash University Elektrolytisk vandopdeli -
 Formskiftende middel er rettet mod skadelige bakterier i mavenKredit:University of Illinois i Urbana-Champaign En ny formskiftende polymer kan målrette og dræbe Helicobacter pylori-bakterier i maven uden at dræbe nyttige bakterier i tarmen. En sådan behandli
Formskiftende middel er rettet mod skadelige bakterier i mavenKredit:University of Illinois i Urbana-Champaign En ny formskiftende polymer kan målrette og dræbe Helicobacter pylori-bakterier i maven uden at dræbe nyttige bakterier i tarmen. En sådan behandli
- Forskellige former for figurer i matematik
- Ny indsigt fra Great Barrier Reef-koraller giver en korrektionsfaktor til klimarekorder
- Kemisk syntese kunne producere mere potente antibiotika
- Lavtemperaturkrystallisation af faserent α-formamidinium blyiodid muliggjort ved undersøgelse
- Hvorfor testede Britains forsvarsministerium psykiske kræfter?
- Seks fod sne i Buffalo:Hvad forårsager søeffektstorme som denne?


