Subatomære partikler:byggestenene mindre end et atom
Af Doug Bennett (Opdateret 30. august 2022)
Mens atomer er de mindste enheder af stof med konsistente egenskaber, ligger det sande grundlag for den fysiske verden i partikler, der er endnu mindre end atomer - subatomære partikler. Disse grundlæggende bestanddele – inklusive protoner, neutroner, elektroner, kvarker og radioaktive alfa- og beta-partikler – sammensætter og afmonterer nogle gange stoffet omkring os.
Protoner
Opdaget af Ernest Rutherford i 1919, protoner bor i atomkerner og bærer en positiv elektrisk ladning. Hver protons masse er groft sagt en atommasseenhed (amu), og sammen med neutroner tegner de sig for det meste af et atoms masse. Antallet af protoner definerer et grundstofs atomnummer.
Neutroner
James Chadwick identificerede neutroner i 1932. Ligesom protoner er neutroner omkring en amu i masse, men er elektrisk neutrale. Variationer i neutrontal giver anledning til isotoper af et enkelt grundstof.
Elektroner
Sir J.J. Thomson observerede først elektroner i 1897. Elektroner kredser om kernen i en elektronsky, som har en masse, der er 1.840 gange mindre end en protons og en negativ ladning. Elektroner driver kemisk binding gennem tab, forstærkning eller deling med andre atomer.
Alfapartikler
Alfa-partikler består af to protoner og to neutroner - kernen i et heliumatom. De udsendes under alfa-henfald af tunge, ustabile kerner. Selvom alfapartikler har lav energi og kort rækkevidde, kan de være yderst skadelige for biologisk væv ved kontakt.
Beta-partikler
Beta-partikler er højenergielektroner (β⁻) eller positroner (β⁺), produceret af beta-henfald. De rejser med hastigheder tæt på lyset og trænger op til 100 gange dybere ind i materialer end alfapartikler.
Quarks
Kvarker er de mindste kendte subatomære enheder og udgør de sande elementære partikler af stof. Seks smagsvarianter - op, ned, charme, mærkelig, top, bund - findes, hver med en af tre "farve" ladninger (rød, blå, grøn). Protoner er lavet af to op og en ned kvark; neutroner omfatter to ned- og en op-kvark.
For mere detaljeret videnskabelig baggrund, se Wikipedia-indlægget om partikler og NIST-definitionen af atommasseenheden .
 Varme artikler
Varme artikler
-
 Forskere introducerer idé til nye molekyler, innovation, værdiLedere fra National Science Foundation Engineering Research Center for Biorenewable Chemicals (CBiRC) baseret på Iowa State University foreslår en ny model til at skabe, ansøger, og kommercialisering
Forskere introducerer idé til nye molekyler, innovation, værdiLedere fra National Science Foundation Engineering Research Center for Biorenewable Chemicals (CBiRC) baseret på Iowa State University foreslår en ny model til at skabe, ansøger, og kommercialisering -
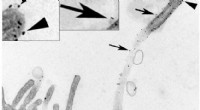 Downstream-signalering:Cilia frigiver ektosomer for at levere vigtige beskeder i nyrenImmunogold mærkning af Exoc5-myc (en komponent i eksocysten) i MDCK-celler viser sorte prikker langs det primære cilium (pilespidser) og tilhørende vesikler (pile). Billedet er taget ved 53, 400X fors
Downstream-signalering:Cilia frigiver ektosomer for at levere vigtige beskeder i nyrenImmunogold mærkning af Exoc5-myc (en komponent i eksocysten) i MDCK-celler viser sorte prikker langs det primære cilium (pilespidser) og tilhørende vesikler (pile). Billedet er taget ved 53, 400X fors -
 Beregn normaliteten af natriumhydroxid (NaOH) - en praktisk vejledningBeregn normaliteten af natriumhydroxid (NaOH) Forfatter: Kittisak Kaewchalun / Getty Images Normalitet er en nøglemetrik i kemi, der udtrykker koncentrationen af en opløsning i form af gramækvivalen
Beregn normaliteten af natriumhydroxid (NaOH) - en praktisk vejledningBeregn normaliteten af natriumhydroxid (NaOH) Forfatter: Kittisak Kaewchalun / Getty Images Normalitet er en nøglemetrik i kemi, der udtrykker koncentrationen af en opløsning i form af gramækvivalen -
 Hvordan temperatur påvirker isbjergsmeltning:en ekspertoversigtDC Productions/Photodisc/Getty Images Forstå isbjergets smeltning Isbjerge, de kolossale flydende masser af ferskvandsis, der driver hen over verdenshavene, er formet af temperaturen på vandet, der o
Hvordan temperatur påvirker isbjergsmeltning:en ekspertoversigtDC Productions/Photodisc/Getty Images Forstå isbjergets smeltning Isbjerge, de kolossale flydende masser af ferskvandsis, der driver hen over verdenshavene, er formet af temperaturen på vandet, der o
- Forskere opdager, at stråling fra massive stjerner former planetsystemer
- Hvad er nogle hverdagsteknologier leveret af NASA Research?
- Beregning af pH af en KOH-opløsning:En trin-for-trin guide
- Fjernelse af CO2 fra luften, der er nødvendig for at sikre børns fremtid
- Sådan fungerer flyforbudszoner
- Hvad er en Marcoburst?


