Dobbelt erstatningsreaktioner forklaret:Hvordan ioner bytter, udfælder eller danner gasser
omega77/iStock/GettyImages
En dobbelterstatningsreaktion (dobbeltforskydning) opstår, når to opløselige salte dissocierer i vand, og deres kationer og anioner udveksler partnere og danner to nye produkter. Reaktionen forløber i vandig opløsning; produkterne kan forblive i opløsning, udvikle sig som en gas eller udfældes som et uopløseligt fast stof.
TL;DR
I en dobbelterstatningsreaktion bytter ioner plads, hvilket fører til enten en udfældning eller en syre-basereaktion. Opløselighedsregler bestemmer, om et fast stof udfældes, en gas udvikler sig, eller om produkterne forbliver i opløsning.
Hvordan reaktionen sker
Overvej to generiske salte, AB og CD. I vand adskilles de til A + + B – og C + + D – . For ligesom ladninger frastøder, rekombinerer kationerne og anionerne for at danne de nye par AD og CB. Afhængigt af deres opløselighed kan AD og CB fremstå som et fast bundfald, forblive opløst eller danne en gas.
Opløselighedsregler
Opløselighedsregler er afgørende for at forudsige resultatet af en dobbelterstatningsreaktion. Hvis en af reaktanterne er uopløselige, vil den ikke deltage. De mest almindeligt anvendte regler er:
- Alt nitrat (NO3 ⁻) salte er opløselige.
- Alkalimetalsalte (Li + , Na + , K + , Rb + , Cs + ) er opløselige.
- Ammonium (NH4 + ) salte er opløselige.
- De fleste halogenidsalte (Cl – , Br – , I – ) er opløselige bortset fra Ag + , Hg2 2+ og Pb 2+ .
- De fleste sulfatsalte (SO4 2– ) er opløselige bortset fra Ca 2+ , Hg2 2+ , Pb 2+ og Ba 2+ .
- De fleste hydroxidsalte er uopløselige undtagen Ca 2+ , Ba 2+ , og Sr 2+ .
- De fleste sulfid-, carbonat-, phosphat- og chromatsalte er uopløselige undtagen salte af alkalimetaller og NH4 + .
Reaktioner med nedbør
Når to opløselige salte blandes, er et almindeligt resultat dannelsen af et uopløseligt fast stof. For eksempel at blande zinknitrat (Zn(NO3 )2 ) og natriumphosphat (Na3 PO4 ) producerer natriumnitrat, som forbliver i opløsning, og zinkphosphat (Zn3 (PO4 )2 ), som udfælder:
Zn(NO3 )2 (aq) + Na3 PO4 (aq) → 3NaNO3 (aq) + Zn3 (PO4 )2 (s)
Sure-base-erstatningsreaktioner
Syrer og baser deltager også i dobbelterstatningsreaktioner. I opløsning donerer en syre H + , mens en base giver OH – . H + og OH – kombineres for at danne vand, og de resterende ioner danner et salt. For eksempel:
HCl (aq) + NaOH (aq) → NaCl (aq) + H2 O (l)
I et mere komplekst tilfælde reagerer natriumcarbonat med saltsyre og giver natriumchlorid, kuldioxidgas og vand:
Na2 CO3 (aq) + 2HCl (aq) → 2NaCl (aq) + CO2 (g) + 3H2 O (l)
Disse eksempler illustrerer, hvordan reaktanternes opløselighed og ionernes identitet bestemmer, om der dannes et bundfald, en gas eller et opløseligt salt.
I tvetydige tilfælde, hvor produkterne forbliver opløselige, kræves der ofte yderligere tests (f.eks. pH-måling, ledningsevne eller spektroskopisk analyse) for at bekræfte, at en reaktion har fundet sted.
 Varme artikler
Varme artikler
-
 Hvorfor bananer er radioaktive - og hvorfor det er helt sikkertHvorfor bananer er radioaktive – og hvorfor det er helt sikkert Det er en almindelig trivia-kendsgerning:bananer indeholder spormængder af radioaktivt kalium. Men niveauet af radioaktivitet er minima
Hvorfor bananer er radioaktive - og hvorfor det er helt sikkertHvorfor bananer er radioaktive – og hvorfor det er helt sikkert Det er en almindelig trivia-kendsgerning:bananer indeholder spormængder af radioaktivt kalium. Men niveauet af radioaktivitet er minima -
 Hvordan temperatur former fugtighed:Et dybt dyk ned i fugt, dugpunkt og fordampningTemperatur og fugt er uadskillelige kræfter i atmosfæren. Når luften opvarmes eller afkøles, ændres mængden af vanddamp, den kan indeholde - og dermed fugtighedsniveauet - tilsvarende. At forstå den
Hvordan temperatur former fugtighed:Et dybt dyk ned i fugt, dugpunkt og fordampningTemperatur og fugt er uadskillelige kræfter i atmosfæren. Når luften opvarmes eller afkøles, ændres mængden af vanddamp, den kan indeholde - og dermed fugtighedsniveauet - tilsvarende. At forstå den -
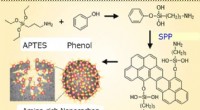 Elektrisk stød til kulstof gør en bedre vandrenserSynteseproces af nanocarbonadsorbent. Kredit:Nagahiro Saito Forskere ved Nagoya University har udviklet en et-trins fremstillingsproces, der forbedrer nanocarbons evne til at fjerne giftige tungme
Elektrisk stød til kulstof gør en bedre vandrenserSynteseproces af nanocarbonadsorbent. Kredit:Nagahiro Saito Forskere ved Nagoya University har udviklet en et-trins fremstillingsproces, der forbedrer nanocarbons evne til at fjerne giftige tungme -
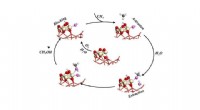 Vand er nøglen til katalytisk omdannelse af methan til methanolKatalytisk cyklus til selektiv omdannelse af methan til methanol ved at udsætte metanen for ilt og vand. Kredit:Brookhaven National Laboratory Forskere ved det amerikanske energiministerium Brookh
Vand er nøglen til katalytisk omdannelse af methan til methanolKatalytisk cyklus til selektiv omdannelse af methan til methanol ved at udsætte metanen for ilt og vand. Kredit:Brookhaven National Laboratory Forskere ved det amerikanske energiministerium Brookh
- En rumstation er formet som en ring og roterer for at simulere tyngdekraften Hvis radius på 110 m m…
- Hvordan luftforurening ændrede sig under COVID-19 i Park City, Utah
- Hvad er mængden af en nanocontainer?
- Er hårdhed en fysisk eller kemisk egenskab?
- Hvad er en videnskabelig definition til bevis?
- Hvilke kræfter får formationer af rockcyklus til at ske?


