En praktisk guide til beregning og blanding af kemiske opløsninger i laboratoriet
Af Douglas Bintzler
Opdateret 30. august 2022
Løsninger baseret på procentdel
Trin 1
Identificer, om koncentrationen er udtrykt som vægt/volumen (w/v) eller volumen/volumen (v/v). En v/v-opløsning involverer typisk et fast stof opløst i en væske, mens en v/v-opløsning involverer blanding af to væsker.
Trin 2
For v/v-fortyndinger skal du anvende fortyndingsligningen C1 V1 =C2 V2 . For eksempel, for at fremstille 100 ml 70 % ethanol fra 95 % ethanol:
95 % × V1 =70 % × 100 ml → V1 =73,6 ml. Tilsæt 26,4 ml vand for at nå 100 ml.
Trin 3
Overfør det flydende opløste stof til en målecylinder eller målekolbe, før der tilsættes opløsningsmiddel. Disse beholdere giver mere præcise volumenaflæsninger end bægre, som er bedre egnede til omtrentlig blanding.
Trin 4
For w/v-opløsninger vejes det faste stof nøjagtigt. En 10 % w/v opløsning indeholder 10 g tørt opløst stof i et slutvolumen på 100 ml. Husk at det opløste stof bidrager til det samlede volumen.
Trin 5
Opløs først det faste opløste stof i en lille mængde opløsningsmiddel for at undgå overdreven brug af opløsningsmiddel. Når den er helt opløst, overføres blandingen til en målecylinder eller målekolbe og tilsæt opløsningsmiddel, indtil det ønskede slutvolumen er nået.
Løsninger beregnet ved hjælp af molaritet
Trin 1
Bestem den fysiske tilstand af det opløste stof. Flydende opløste stoffer kommer ofte med en specificeret molaritet og kræver muligvis kun fortynding. Faste opløste stoffer kræver nøjagtig vejning.
Trin 2
Brug fortyndingsligningen for flydende opløste stoffer. For at fortynde 5M NaCl til 1M i 100mL:
5M × V1 =1M × 100mL → V1 =20 ml. Tilsæt 80mL vand.
Trin 3
Fortsæt som i trin 3 i procentdelen:Hæld det flydende opløste stof i en målecylinder eller målekolbe, og tilsæt derefter opløsningsmiddel for at opnå målvolumen.
Trin 4
Identificer den molære masse (MW) af det faste opløste stof. MW er anført på beholderen eller i MSDS. For NaCl, MW=58,4g/mol, hvilket betyder, at 58,4g opløst i 1L giver en 1M opløsning.
Trin 5
Beregn massen af opløst stof, der er nødvendig for den ønskede molaritet ved hjælp af masse=MW × molaritet × volumen (L) . En 2M NaCl-opløsning i 1L kræver 58,4g×2=116,8g.
Trin 6
Juster beregningen for det eksperimentelle volumen. For 100mL (0,1L) 2M NaCl er den nødvendige masse 0,1L×116,8g=11,68g.
Trin 7
Opløs først det faste stof i en lille mængde opløsningsmiddel, overfør derefter til en målecylinder eller målekolbe og tilsæt yderligere opløsningsmiddel, indtil det endelige volumen er opnået.
Justering af opløsningens pH
Trin 1
Mål pH med et kalibreret pH-meter for nøjagtighed; pH-papir kan bruges, hvis en måler ikke er tilgængelig. For eksempel giver NaCl i vand typisk en neutral pH på 7.
Trin 2
Sammenlign den målte pH med målværdien. Hvis opløsningen er for basisk (pH>7) eller for sur (pH<7), skal du justere i overensstemmelse hermed.
Trin 3
Tilsæt en fortyndet syre (f.eks. 0,1 M HCl) for at sænke pH eller en fortyndet base (f.eks. 0,1 M NaOH) for at hæve pH. Brug små trin for at undgå overskridelse; disse reagenser ændrer minimalt opløsningens sammensætning.
Ting, der er nødvendige
- Analytisk balance
- Klassificerede cylindre
- Turgangsbæger eller Erlenmeyer-kolbe
- pH-måler eller pH-indikatorpapir
- Volumetrisk kolbe
TL;DR
Brug målekolber til præcise volumenmålinger. Graduerede cylindre er acceptable erstatninger. Bægerglas og Erlenmeyer-kolber er velegnede til blanding, men mindre nøjagtige for det endelige volumen.
Sikkerhedsadvarsel
Bær altid passende øjenbeskyttelse og, når det er nødvendigt, et stinkskab. Syrer, baser og andre kemikalier kan afgive skadelige dampe. Se MSDS - normalt leveret sammen med kemikaliet eller tilgængelig online - for detaljerede sikkerhedsinstruktioner.
Sidste artikelSådan bestemmes rækkefølgen af en kemisk reaktion
Næste artikelTilskuerioner:deres rolle og eksempler i kemiske reaktioner
 Varme artikler
Varme artikler
-
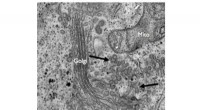 Enzym har vist sig at kontrollere dannelsen af kollagenbærere og hæmme kollagensekretionElektronmikroskopi-billeddannelse afslører tilstedeværelsen af mange indbyrdes forbundne vesikler, som ser ud til at opføre sig som kollagenbærere (angivet med pile). Kredit: Biokemisk og biofysisk
Enzym har vist sig at kontrollere dannelsen af kollagenbærere og hæmme kollagensekretionElektronmikroskopi-billeddannelse afslører tilstedeværelsen af mange indbyrdes forbundne vesikler, som ser ud til at opføre sig som kollagenbærere (angivet med pile). Kredit: Biokemisk og biofysisk -
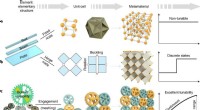 Gear-baserede mekaniske metamaterialer giver mulighed for oprettelse af konfigurerbare arkDesignkoncepter af mekaniske metamaterialer. a,b, klassisk paradigme:ikke-afstembart metamateriale (a) og typisk rekonfigurerbart metamateriale (b). c, Gear-baserede metamaterialer. Kredit:Nature Mate
Gear-baserede mekaniske metamaterialer giver mulighed for oprettelse af konfigurerbare arkDesignkoncepter af mekaniske metamaterialer. a,b, klassisk paradigme:ikke-afstembart metamateriale (a) og typisk rekonfigurerbart metamateriale (b). c, Gear-baserede metamaterialer. Kredit:Nature Mate -
 Forbedret proteinfunktion åbner vej for nyt koncept for lægemiddeludviklingKredit:CC0 Public Domain Forskere ved Karolinska Institutet og SciLifeLab i Sverige beskriver i en undersøgelse offentliggjort i Science hvordan de har forbedret et proteins evne til at reparere ox
Forbedret proteinfunktion åbner vej for nyt koncept for lægemiddeludviklingKredit:CC0 Public Domain Forskere ved Karolinska Institutet og SciLifeLab i Sverige beskriver i en undersøgelse offentliggjort i Science hvordan de har forbedret et proteins evne til at reparere ox -
 Team opnår to-elektron kemiske reaktioner ved hjælp af lysenergi, guldUnder de rette forhold, guld nanopartikler absorberer lys og overfører elektroner til andre reaktanter. Denne proces kan bruges til at omdanne CO2 og vand til kulbrinter. I grafikken, kulstofatomer er
Team opnår to-elektron kemiske reaktioner ved hjælp af lysenergi, guldUnder de rette forhold, guld nanopartikler absorberer lys og overfører elektroner til andre reaktanter. Denne proces kan bruges til at omdanne CO2 og vand til kulbrinter. I grafikken, kulstofatomer er


