Sådan bestemmes rækkefølgen af en kemisk reaktion
I kemisk kinetik beskriver reaktionshastigheden, hvor hurtigt reaktanter omdannes til produkter. takstloven udtrykker dette forhold matematisk ved at inkorporere en hastighedskonstant og eksponenter, der repræsenterer reaktionsrækkefølgen med hensyn til hver reaktant. At bestemme disse eksponenter eksperimentelt er afgørende for at forstå reaktionsmekanismer og optimere industrielle processer.
TL;DR
Mål den indledende hastighed for produktdannelse, mens de indledende koncentrationer eller tryk af hver reaktant varieres. Plot dataene for at identificere, hvordan hastigheden skalerer med hver komponent, afslører reaktionsrækkefølgen og muliggør beregning af hastighedskonstanten.
Forstå reaktionsordren
Rækkefølgen af en reaktion refererer til den effekt, som koncentrationen af hver reaktant er hævet til i hastighedsloven. Det er ikke det samme som den støkiometriske koefficient i den balancerede ligning; snarere afspejler det hastighedens følsomhed over for ændringer i koncentrationen.
- Nulorden :Hastigheden er uafhængig af reaktantkoncentration(er). Eksempel:r =k.
- Første ordre :Hastigheden er direkte proportional med koncentrationen af en reaktant. Eksempel:r =k[A].
- Anden orden :Hastigheden afhænger af kvadratet af en reaktantkoncentration eller produktet af to reaktantkoncentrationer. Eksempel:r =k[A][B] eller r =k[A]².
Nulordreaktioner
I en ægte nulteordensreaktion forbliver reaktionshastigheden konstant over tid, forudsat at reaktanterne er til stede. Grafisk falder koncentrationen af en reaktant lineært med tiden, mens produktkoncentrationen stiger lineært. Hældningen af disse linjer er lig med hastighedskonstanten k, men k er ikke en funktion af reaktantkoncentrationen.
I praksis forekommer mange reaktioner af nulte orden under specifikke forhold - såsom enzymkatalyserede reaktioner ved mættende substratniveauer eller overflademedierede processer, hvor den aktive overflade bliver en begrænsende faktor. Disse omtales ofte som pseudo-nulorden fordi antagelsen kun gælder indtil en reaktant er opbrugt.
Bestemmelse af reaktionsrækkefølge og ratekonstant
Nøjagtig kinetisk analyse er afhængig af initial-rate-metoden . Følg disse trin:
- Opsæt en række identiske reaktioner, hver med en forskellig startkoncentration (eller tryk) af én reaktant, mens andre holdes konstante.
- Mål hastigheden af produktdannelse helt i starten af hver reaktion – før der sker et betydeligt forbrug af reaktanter.
- Plot starthastighederne (r) mod startkoncentrationerne ([A], [B], osv.).
- Hvis plottet er en ret linje gennem origo, giver hældningen hastighedskonstanten og rækkefølgen (hældning =1 for første orden).
- Et logaritmisk plot (logr vs. log[A]) giver rækkefølgen som linjens hældning.
- Krumte plots indikerer mere komplekse mekanismer eller højere ordens afhængighed.
- Bekræft den afledte hastighedslov ved at sammenligne forudsagte koncentrationer over tid med eksperimentelle data ved hjælp af integration eller numeriske metoder.
Typiske faldgruber omfatter:
- Brug af gennemsnitlige koncentrationer i stedet for startværdier, som kan maskere ægte kinetisk adfærd.
- Hvis man ignorerer ændringer i temperatur, tryk eller katalysatoroverfladeareal, der ændrer den effektive hastighedskonstanten.
- Forudsat en enkelttrinsmekanisme, når reaktionen forløber gennem mellemprodukter.
For visuelle elever demonstrerer en kortfattet YouTube-selvstudie af Dr. Kim ved MIT den indledende satsmetode med rigtige datasæt:https://www.youtube.com/watch?v=example .
Billedkredit:SARINYAPINNGAM/iStock/GettyImages
 Varme artikler
Varme artikler
-
 Optiske overtoner til solcellerAnalogt med et fænomen kendt for musikinstrumenter, når overtoner af to forskellige grundtoner kommer i resonans, forskere fra LMU München har fundet en ny effekt med hensyn til optisk excitation af l
Optiske overtoner til solcellerAnalogt med et fænomen kendt for musikinstrumenter, når overtoner af to forskellige grundtoner kommer i resonans, forskere fra LMU München har fundet en ny effekt med hensyn til optisk excitation af l -
 Forvandling af træ til plastikKredit:Unsplash/CC0 Public Domain Bestræbelser på at skifte fra petrokemisk plast til vedvarende og bionedbrydelig plast har vist sig vanskelig - produktionsprocessen kan kræve giftige kemikalier
Forvandling af træ til plastikKredit:Unsplash/CC0 Public Domain Bestræbelser på at skifte fra petrokemisk plast til vedvarende og bionedbrydelig plast har vist sig vanskelig - produktionsprocessen kan kræve giftige kemikalier -
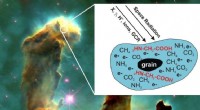 Hvordan livets byggesten kan dannes i rummetElektroner med lav energi skabt i stof af rumstråling (f.eks. galaktiske kosmiske stråler, GCR, etc.), kan inducere dannelse af glycin (2HN-CH2-COOH) i astrofysiske molekylære iser; her, iskolde korn
Hvordan livets byggesten kan dannes i rummetElektroner med lav energi skabt i stof af rumstråling (f.eks. galaktiske kosmiske stråler, GCR, etc.), kan inducere dannelse af glycin (2HN-CH2-COOH) i astrofysiske molekylære iser; her, iskolde korn -
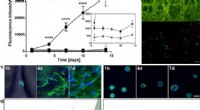 Engineering ECM-lignende fibre med bioaktiv silke til 3-D cellekulturSpredning og udvidelse af celler i FN-silke sammenlignet med når de er indkapslet i en RGD-koblet hydrogel. (a) repræsentativ graf (middelværdi og standardafvigelse) for Alamar Blue-levedygtighedsassa
Engineering ECM-lignende fibre med bioaktiv silke til 3-D cellekulturSpredning og udvidelse af celler i FN-silke sammenlignet med når de er indkapslet i en RGD-koblet hydrogel. (a) repræsentativ graf (middelværdi og standardafvigelse) for Alamar Blue-levedygtighedsassa
- Hvad er et stort problem, der er forbundet med brugen af kul med højt svovlindhold som brændsel?…
- Hvordan er loven om bevaringsenergi og masse ens?
- Hvad er produktet, når natriumcarbonat reagerer med calciumchlorid?
- Gamle hunde:Forudgående viden påvirker, hvordan forbrugerne accepterer ny information
- Hvordan er erosion nyttig?
- Hvordan har COVID-19 ændret superstjernebyer?


