Elektronisk geometri vs. molekylær form:nøgleforskelle forklaret
Af Rosann Kozlowski Opdateret 30. august 2022
DragonImages/iStock/GettyImages
Elektronisk geometri og molekylær form beskriver, hvordan elektroner og atomer er placeret omkring et centralt atom i det tredimensionelle rum og bestemmer molekylets form og bindingsvinkler.
Definitioner:Elektronisk geometri vs. molekylær form
Elektronisk geometri refererer til arrangementet af elektrongrupper - både bindingspar og ensomme par - omkring et centralt atom. Molekylær form beskriver på den anden side kun det rumlige arrangement af de bundne atomer. Når et molekyle ikke indeholder ensomme par, falder de to begreber sammen; ellers forvrænger ensomme par formen.
VSEPR-teori og dens rolle i at forudsige geometri
Valence-Shell Electron-Pair Repulsion (VSEPR) modellen forudsiger geometrien af et molekyle ved at minimere frastødning blandt elektronpar. Ensomme par frastøder stærkere end bindingspar, hvilket reducerer bindingsvinklerne en smule sammenlignet med de ideelle værdier for en given elektronisk geometri.
Elektronisk geometri efter antal elektrongrupper
- 2 grupper:lineær (180°)
- 3 grupper:trigonal plan (120°)
- 4 grupper:tetraedrisk (109,5°)
- 5 grupper:trigonal bipyramidal (120°/90°)
- 6 grupper:oktaedrisk (90°)
Almindelige former afledt af hver elektronisk geometri
Nedenfor er de typiske molekylære former, der opstår, når ensomme par optager elektrongrupperne. Formen, der er angivet først for hver geometri, er den eneste, hvor elektronisk geometri og molekylær form matcher.
Lineær (2 grupper)
- Lineær – 180° (elektrongeometri =molekylær form)
Trigonal Planar (3 grupper)
- Trigonal plan – 120° (ingen enlige par)
- Bøjet – 2 bindinger, 1 enkelt par (bindingsvinkel <120°)
Tetrahedral (4 grupper)
- Tetrahedral – 109,5° (ingen enlige par)
- Trigonal pyramideformet – 3 bindinger, 1 ensomt par (bindingsvinkel <109,5°)
- Bøjet – 2 bindinger, 2 ensomme par (bindingsvinkel <109,5°)
Trigonal Bipyramidal (5 grupper)
- Trigonal bipyramidal – 120°/90° (ingen ensomme par)
- Vippe – 4 bindinger, 1 ensomt par (enlige par indtager aksial position)
- T-formet – 3 bindinger, 2 enlige par
- Lineær – 2 bindinger modsat hinanden, 3 ensomme par
Oktaedral (6 grupper)
- Oktaedrisk – 90° (ingen enlige par)
- Kvadratisk pyramideformet – 5 bindinger, 1 ensomt par (enligt par indtager aksial position)
- Kvadratisk plan – 4 bindinger, 2 enlige par (enlige par indtager aksiale positioner)
Disse forhold gør det muligt for kemikere at forudsige både formen af et molekyle og dets bindingsvinkler ud fra en simpel optælling af elektronpar.
 Varme artikler
Varme artikler
-
 Forskere forbedrer cykelydelsen af Al-baserede batterier med katode med høj arealdensitetAl-anode i lithium-ion-batteri med høj arealdensitet, strukturen er stensikker som Great Wall Credit:SIAT Lithium-ion-batterier (LIBer) er den dominerende strømkilde til bærbar elektronik og elekt
Forskere forbedrer cykelydelsen af Al-baserede batterier med katode med høj arealdensitetAl-anode i lithium-ion-batteri med høj arealdensitet, strukturen er stensikker som Great Wall Credit:SIAT Lithium-ion-batterier (LIBer) er den dominerende strømkilde til bærbar elektronik og elekt -
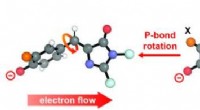 Hvordan elektriske felter påvirker et molekylært twist i lysfølsomme proteinerNår lys rammer visse kromoforer i proteiner, det får dem til at vride sig og ændre form. Denne atomare rekonfiguration, kendt som fotoisomerisering, ændrer molekylets kemiske og fysiske egenskaber. Ke
Hvordan elektriske felter påvirker et molekylært twist i lysfølsomme proteinerNår lys rammer visse kromoforer i proteiner, det får dem til at vride sig og ændre form. Denne atomare rekonfiguration, kendt som fotoisomerisering, ændrer molekylets kemiske og fysiske egenskaber. Ke -
 Grønt protein uden smag af kostaldKredit:Miriam Meister Forskere fra DTU Fødevarer har udviklet en teknik til at udvinde protein fra grøn biomasse uden uønsket bismag. Køer kan lide græs for at smage som græs. Imidlertid, hvis fo
Grønt protein uden smag af kostaldKredit:Miriam Meister Forskere fra DTU Fødevarer har udviklet en teknik til at udvinde protein fra grøn biomasse uden uønsket bismag. Køer kan lide græs for at smage som græs. Imidlertid, hvis fo -
 Forskere skaber en ny elektronegativitetsskalaKredit:Pixabay/CC0 Public Domain Skoltech-kemikere har foreslået en ny elektronegativitetsskala og offentliggjort deres resultater i Naturkommunikation . Begrebet elektronegativitet introducere
Forskere skaber en ny elektronegativitetsskalaKredit:Pixabay/CC0 Public Domain Skoltech-kemikere har foreslået en ny elektronegativitetsskala og offentliggjort deres resultater i Naturkommunikation . Begrebet elektronegativitet introducere
- SF-cellelukning:Sikkerhedsproblem eller antydning af Orwell? (Opdatering)
- Hvad er valensen af aluminiumborat?
- Hvor succesrige er supersparebegivenheder med detailhandlertema?
- Solarovne Vs. Konventionelle ovne
- Hvor mange joules arbejde udføres, når en Force 1 N bevæger bog 2m?
- Bytte en fusion med bredbånd?


