Identifikation af den begrænsende reaktant i støkiometri:En praktisk vejledning
Af Riti Gupta
Opdateret 30. august 2022
Hvad er en begrænsende reaktant?
I en kemisk reaktion stopper den reaktant, der først er fuldstændigt forbrugt, reaktionen. Denne reaktant er kendt som den begrænsende reaktant (eller begrænsende reagens). Den resterende reaktant, hvis nogen, kaldes overskydende reaktant .
Hvorfor det betyder noget
I de fleste laboratorieindstillinger tilsættes reaktanter i mængder, der ikke svarer til de nøjagtige støkiometriske forhold vist i den afbalancerede ligning. At forstå, hvilke arter der begrænser, hjælper kemikere med at forudsige produktudbytte, designe opskaleringsprocesser og undgå dyrt spild.
Eksempel 1:Ammoniak og kuldioxid til urinstof
Den afbalancerede ligning for urinstofsyntese er:
\(2\mathrm{NH}_3(g)+\mathrm{CO}_2(g) \højrepil (\mathrm{NH}_2)_2\mathrm{CO}(aq)+\mathrm{H}_2\mathrm{O}(l)\)
Ud fra koefficienterne reagerer 2mol ammoniak med 1mol kuldioxid. Antag, at vi tilføjer 4mol \(\mathrm{CO}_2\) og 12mol \(\mathrm{NH}_3\).
Beregn den nødvendige ammoniak til 4mol kuldioxid:
\(4\text{ mol }\mathrm{CO}_2\left(\dfrac{2\text{ mol }\mathrm{NH}_3}{1\text{ mol }\mathrm{CO}_2}\right)=8\text{ mol }\mathrm{NH}_3\)
Der kræves kun 8 mol ammoniak, hvilket efterlader 4 mol ubrugt. Derfor er kuldioxid den begrænsende reaktant, og ammoniak er i overskud.
Alternativt kan du bestemme, hvor meget kuldioxid der skal til for 12 mol ammoniak:
\(12\text{ mol }\mathrm{NH}_3\left(\dfrac{1\text{ mol }\mathrm{CO}_2}{2\text{ mol }\mathrm{NH}_3}\right)=6\text{ mol }\mathrm{CO}_2\)
Fordi kun 4 mol \(\mathrm{CO}_2\) er til stede, følger den samme konklusion:kuldioxid begrænser reaktionen.
Eksempel 2:Fremstilling af aluminiumklorid
Den afbalancerede ligning er:
\(2\mathrm{Al}+3\mathrm{Cl}_2 \højrepil 2\mathrm{AlCl}_3\)
Givet 25 g aluminium og 32 g klorgas, konverter masser til mol:
Aluminium:\(25\text{ g }\mathrm{Al}\left(\dfrac{1\text{ mol }\mathrm{Al}}{26.98\text{ g }\mathrm{Al}}\right)=0.93\text{ mol }\mathrm{Al}\)
Klor:\(32\text{ g }\mathrm{Cl}_2\left(\dfrac{1\text{ mol }\mathrm{Cl}_2}{70,90\text{ g}\mathrm{Cl}_2}\right)=0,45\text{ mol }\mathrm{Cl}_2\)
Bestem det klor, der kræves for at forbruge alt aluminium:
\(0,93\text{ mol }\mathrm{Al}\left(\dfrac{3\text{ mol }\mathrm{Cl}_2}{2\text{ mol }\mathrm{Al}}\right)=1,40\text{ mol }\mathrm{Cl}_2\)
Kun 0,45 mol klor er tilgængelig, så klor er den begrænsende reaktant. Den overskydende reaktant er aluminium.
Verifikation:Der er brug for mol aluminium til al klor:
\(0,45\text{ mol }\mathrm{Cl}_2\left(\dfrac{2\text{ mol }\mathrm{Al}}{3\text{ mol }\mathrm{Cl}_2}\right)=0,30\text{ mol }\mathrm{Al}\)
Da der er 0,93 mol aluminium til stede, forbliver konklusionen uændret.
Nøgletilbehør
Den begrænsende reaktant bestemmes af de faktiske mængder af anvendte reaktanter, ikke af de støkiometriske koefficienter alene. Beregning af forholdet mellem tilgængelige mol og det støkiometriske forhold vil altid afsløre, hvilken art der begrænser produktdannelsen.
Sidste artikelFem nøgleeksempler på kemisk forvitring og deres miljøpåvirkning
Næste artikelJ.J. Thomson:Pioner inden for moderne atomteori
 Varme artikler
Varme artikler
-
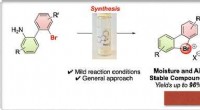 Cykliske hypervalente brom virker som aryne forstadierKredit:Wiley Diaryl λ 3 -bromaner er en sjælden og generelt uforsket klasse af forbindelser. En mild og effektiv protokol leverer nu en bred palet af disse interessante byggesten til organisk sy
Cykliske hypervalente brom virker som aryne forstadierKredit:Wiley Diaryl λ 3 -bromaner er en sjælden og generelt uforsket klasse af forbindelser. En mild og effektiv protokol leverer nu en bred palet af disse interessante byggesten til organisk sy -
 Elektrostatisk kontrollerede overfladegrænseforhold i nematiske flydende krystaller og kolloiderKarakterisering af blodpladernes størrelse og orientering i nematisk LC. SEM-mikrofotografier af blodplader før (A) og efter (B) SiO2-coating. (C) TEM mikroskop af partikler. Indsatsen viser SiO2-lage
Elektrostatisk kontrollerede overfladegrænseforhold i nematiske flydende krystaller og kolloiderKarakterisering af blodpladernes størrelse og orientering i nematisk LC. SEM-mikrofotografier af blodplader før (A) og efter (B) SiO2-coating. (C) TEM mikroskop af partikler. Indsatsen viser SiO2-lage -
 Softwareprogrammet Allchemy identificerer præbiotisk syntese af biokemiske forbindelser fra urpræk…Et team af forskere, der arbejder i Institut for Organisk Kemis laboratorium på det polske videnskabsakademi, har udviklet et softwareprodukt til at hjælpe med at opdage de kemiske processer, der ført
Softwareprogrammet Allchemy identificerer præbiotisk syntese af biokemiske forbindelser fra urpræk…Et team af forskere, der arbejder i Institut for Organisk Kemis laboratorium på det polske videnskabsakademi, har udviklet et softwareprodukt til at hjælpe med at opdage de kemiske processer, der ført -
 Mestring af molaritet:En trin-for-trin guide til beregning af molar koncentrationAf Chris Deziel Opdateret 30. august 2022 En opløsning er en homogen blanding, hvor et opløst stof er dispergeret i et opløsningsmiddel. I de fleste hverdagsopløsninger tjener vand som opløsningsmid
Mestring af molaritet:En trin-for-trin guide til beregning af molar koncentrationAf Chris Deziel Opdateret 30. august 2022 En opløsning er en homogen blanding, hvor et opløst stof er dispergeret i et opløsningsmiddel. I de fleste hverdagsopløsninger tjener vand som opløsningsmid
- Skal jeg som tiende klassetrin dobbeltarbejde matematik for at hjælpe mig med at blive en dyrlæge?…
- NASA arbejder på at give satellitsværme en bikube
- Hvad er placeringen af clostridium tetani?
- Bosch:Vil lidar -teknologien dreje et hjørne til autonom kørsel?
- Hvad er tre naturlige processer, der måske har bidraget til at forme jorden?
- Nyt kort for radioaktiv jordforurening i Vesteuropa


