Mestring af molaritet:En trin-for-trin guide til beregning af molar koncentration
Af Chris Deziel
Opdateret 30. august 2022
En opløsning er en homogen blanding, hvor et opløst stof er dispergeret i et opløsningsmiddel. I de fleste hverdagsopløsninger tjener vand som opløsningsmiddel, og det opløste stof bestemmer opløsningens egenskaber. Kemikere har brug for en præcis måde at beskrive koncentrationen af opløst stof på, og den mest udbredte enhed er molaritet (M) , defineret som antallet af mol opløst stof pr. liter opløsning.
Hvad er en muldvarp?
Muldvarpen er en grundlæggende måling i kemi, forankret ved Avogadros tal (6.022 × 10 23 atomer eller molekyler). Et mol af ethvert stof har en masse, i gram, lig med dets molære masse (atom- eller molekylvægten i atommasseenheder). For eksempel er brints atommasse 1,008 amu, så et mol brint vejer 1,008 gram.
For at bestemme molmassen af en forbindelse skal du tilføje atommasserne af alle atomer i dens formel (findes i det periodiske system). Når du har den molære masse, kan du konvertere en vejet prøve til mol ved at dividere dens masse med den molære masse.
Eksempel:Natriumhydroxid (NaOH)
Na (22,990 g/mol), O (15,999 g/mol), H (1,008 g/mol). Molmasse =22.990 + 15.999 + 1.008 ≈ 40,0 g/mol. En prøve på 32 gram indeholder 32 g ÷ 40,0 g/mol ≈ 0,80 mol.
Sådan beregnes molaritet
Med kendte mol af opløst stof har du brug for opløsningens volumen i liter. Hvis du måler volumen i en anden enhed, konverter den ved hjælp af:
- 1 liter = 0,001 m 3 = 1.000 mL = 0,264 US gallon = 33,81 væske ounces
Molaritet (M) = mol opløst stof ÷ liter opløsning.
Illustrativt eksempel:Salt i vand
Beregn molariteten af en opløsning fremstillet ved at opløse 12 g natriumchlorid (NaCl) i 20 oz vand.
1. Mol NaCl
Na (23,0 g/mol) + Cl (35,5 g/mol) = 58,5 g/mol. Mol =12 g ÷ 58,5 g/mol ≈ 0,205 mol.
2. Konverter volumen til liter
20 oz ÷ 33,81 oz/L ≈ 0,592 L.
3. Beregn molaritet
0,205 mol ÷ 0,592 L ≈ 0,35 M.
Den resulterende opløsning har således en molaritet på ca. 0,35 M.
 Varme artikler
Varme artikler
-
 Forskere øger varmen på smeltede metaller for at skabe fremtidige teknologierBryan Owens-Baird, en kandidatstuderende forsker fra Iowa State University, forbereder sig på at studere en af sine prøver, en pulveriseret forbindelse af fosfor, silicium, og tin, med NOMAD -instru
Forskere øger varmen på smeltede metaller for at skabe fremtidige teknologierBryan Owens-Baird, en kandidatstuderende forsker fra Iowa State University, forbereder sig på at studere en af sine prøver, en pulveriseret forbindelse af fosfor, silicium, og tin, med NOMAD -instru -
 Detaljeret fotodissociationsdynamik af hydrogensulfid afsløretRotations- og nuklear-spin-niveauafhængig multi-kanal produktmåling og fotodissociationsmekanismer af H 2 S. Kredit:ZHAO Yarui og YUAN Kaijun Svovlbrinte (H 2 S) er et af de vigtigste molekyle
Detaljeret fotodissociationsdynamik af hydrogensulfid afsløretRotations- og nuklear-spin-niveauafhængig multi-kanal produktmåling og fotodissociationsmekanismer af H 2 S. Kredit:ZHAO Yarui og YUAN Kaijun Svovlbrinte (H 2 S) er et af de vigtigste molekyle -
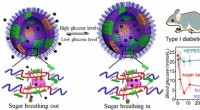 Sukkersvampe suger op og frigiver glukose efter behovKredit:American Chemical Society Mange diabetespatienter skal injicere sig selv med insulin, nogle gange flere gange om dagen, mens andre tager medicin oralt for at kontrollere blodsukkeret. Indsp
Sukkersvampe suger op og frigiver glukose efter behovKredit:American Chemical Society Mange diabetespatienter skal injicere sig selv med insulin, nogle gange flere gange om dagen, mens andre tager medicin oralt for at kontrollere blodsukkeret. Indsp -
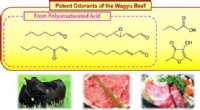 Nøgle lugtstoffer i verdens dyreste oksekød kunne hjælpe med at forklare dens tiltrækningKredit:American Chemical Society Kendt for sin bløde tekstur og karakteristiske smag, Wagyu-oksekød - ofte omtalt som Kobe-oksekød i USA - er blevet et af verdens mest eftertragtede kød. Nu i en u
Nøgle lugtstoffer i verdens dyreste oksekød kunne hjælpe med at forklare dens tiltrækningKredit:American Chemical Society Kendt for sin bløde tekstur og karakteristiske smag, Wagyu-oksekød - ofte omtalt som Kobe-oksekød i USA - er blevet et af verdens mest eftertragtede kød. Nu i en u
- Hvad er den kraft, du udøver, når du bruger en maskine?
- Hvorfor skulle en supergiant have lysere absolut magintude end hvid dværg?
- Hvis en kasse er stationær på en hældning, betyder det, at i ligevægtstilstanden?
- Er scoria og rhyolit det samme i mineralsammensætning?
- Hvad er intermolekylære brintbindinger?
- CyLab-forskere foreslår nye regler for retfærdighed på internettet


