Inde i et atom:Placeringen af protoner, neutroner og elektroner
Af Neha Tripathi Opdateret 24. marts 2022
Ben-Schonewille/iStock/Getty Images
Strukturen af et atom kan visualiseres som et miniature solsystem. Elektroner kredser om den tætte kerne ligesom planeter kredser om solen. Mens tyngdekraften holder planeter sammen, er kræfterne, der binder et atom, elektromagnetisk tiltrækning og den stærke kernekraft.
Kerne
Kernen sidder i midten af hvert atom og indeholder protoner og neutroner. Antallet af protoner - dets atomnummer - definerer grundstoffet; helium har altid to protoner, kulstof seks, og så videre. Isotoper af samme grundstof opstår, når neutrontallet varierer; de fleste brintatomer har ingen neutroner, men sjældne former bærer en eller to. Den stærke kernekraft, en fundamental vekselvirkning, holder protoner og neutroner bundet inde i kernen.
Protoner
Protoner er de eneste positivt ladede subatomære partikler i et atom. Hver bærer en ladning på +1,6022×10⁻¹⁹ coulombs, svarende til en elektrons negative ladning. Med en masse på 1,67×10⁻²⁷ kilogram er en proton cirka 1.837 gange tungere end en elektron og næsten lige så tung som en neutron.
Elektroner
Elektroner, betegnet med symbolet e⁻, er de eneste negativt ladede partikler i et atom. Deres masse er kun 1,1×10⁻³¹ kilogram. Elektroner optager diskrete energiskaller, der omgiver kernen; hver skal har en begrænset kapacitet (2, 8, 18, 32, …), der bestemmer atomets kemiske adfærd. Fordi skallerne ligger langt fra kernen, består atomer af mere end 99 % tomt rum.
Neutroner
Neutroner er neutrale partikler, der deler kernen med protoner. Alle grundstoffer undtagen brint indeholder mindst én neutron. En neutrons masse er 1,6749×10⁻²⁷ kilogram, næsten identisk med en protons. Ved radioaktivt henfald kan en neutron udsendes og vandre frit i omkring 15 minutter, før den omdannes til en proton og en elektron.
Sidste artikelFjernelse af fugt fra naturgas:en teknisk oversigt
Næste artikelSådan øges vandets pH-værdi sikkert med bagepulver
 Varme artikler
Varme artikler
-
 Overfladeteknik får rødt lysPassivering af overfladen af perovskit nanokrystaller med IDA-molekyler forbedrer deres stabilitet og deres optiske og elektriske egenskaber, gør dem nyttige til optoelektroniske enheder. Kredit:KAU
Overfladeteknik får rødt lysPassivering af overfladen af perovskit nanokrystaller med IDA-molekyler forbedrer deres stabilitet og deres optiske og elektriske egenskaber, gør dem nyttige til optoelektroniske enheder. Kredit:KAU -
 Bare tilsæt vand - Kemikere afslører en mekanisme bag doping af organiske halvledereDenne Lewis-syre ændrer de elektriske egenskaber af visse organiske halvledere, når den tilsættes i tilstedeværelsen af vand Kredit: Brett Yurash Halvledere – og vores beherskelse af dem – har g
Bare tilsæt vand - Kemikere afslører en mekanisme bag doping af organiske halvledereDenne Lewis-syre ændrer de elektriske egenskaber af visse organiske halvledere, når den tilsættes i tilstedeværelsen af vand Kredit: Brett Yurash Halvledere – og vores beherskelse af dem – har g -
 Vand-i-salt elektrolyt giver stabil katode til lithium-luft batteridriftAfladet kulstofkatode set gennem scanningselektronmikroskopi af et hold forskere fra Boston College og Danmarks Tekniske Universitet. De energilagrende knuder i nærvær af vandmolekyler afspejler en el
Vand-i-salt elektrolyt giver stabil katode til lithium-luft batteridriftAfladet kulstofkatode set gennem scanningselektronmikroskopi af et hold forskere fra Boston College og Danmarks Tekniske Universitet. De energilagrende knuder i nærvær af vandmolekyler afspejler en el -
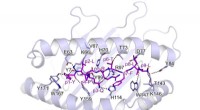 Afdækning af, hvordan T-celler genkender SARS-COV-2 virus spike proteinStruktur af HLA-A2S269-277. H-bindingsinteraktioner mellem S269-277-peptidet (lilla pinde) og HLA-A2 (tegneserie). HLA-A2-kontaktrester og H-bindinger inden for 3,5 Å af peptidet er vist (lyseblå pind
Afdækning af, hvordan T-celler genkender SARS-COV-2 virus spike proteinStruktur af HLA-A2S269-277. H-bindingsinteraktioner mellem S269-277-peptidet (lilla pinde) og HLA-A2 (tegneserie). HLA-A2-kontaktrester og H-bindinger inden for 3,5 Å af peptidet er vist (lyseblå pind
- Den nukleare rolle i reguleringen af genekspression involverer?
- Hvorfor moderne regeringer alle har brug for et ministerium for oceanerne
- Sådan fungerer røghoppere
- Amazon og Lidl skaber omvæltning for store Charlotte-købmænd, viser ny rapport
- Spanien sætter temperaturrekorder, Storbritannien ser den varmeste dag i 2020
- Hvor succesrige er supersparebegivenheder med detailhandlertema?


