Sådan identificeres en isotop:En praktisk vejledning
Af Drew Lichtenstein
Opdateret 24. marts 2022
Emilija Randjelovic/iStock/GettyImages
Isotoper er atomer af det samme kemiske element, der adskiller sig i neutronantal, hvilket fører til forskellige atommasser. Mens de fleste isotoper er stabile, er nogle radioaktive og udsender stråling, når de henfalder. Neutroner, som ikke bærer nogen ladning, opholder sig i kernen sammen med protoner og bidrager til et atoms masse og strukturelle stabilitet. I det periodiske system er atommassetallet lig med summen af protoner og neutroner.
Trin 1
Bestem neutrontallet for det pågældende atom. I praksis er denne værdi leveret i eksperimentelle data eller databaser, da det er både upraktisk og dyrt at inspicere individuelle atomer direkte.
Trin 2
Se det periodiske system og bemærk grundstoffets standard atommasse. Pålidelige kilder såsom NIST Atomic Weights-databasen giver præcise værdier.
Trin 3
Træk antallet af protoner (atomnummeret) fra standard atommassen for at opnå det typiske neutrontal for det element. Hvis det neutrontal, du målte, afviger fra denne værdi, er atomet en isotop.
For detaljerede eksempler og avancerede applikationer, se IUPAC-retningslinjer eller peer-reviewed litteratur i nuklear kemi.
Sidste artikelElektronpartal:Nøglen til molekylær geometri
Næste artikelSkab en præcis 1 % saccharoseopløsning – trin-for-trin guide
 Varme artikler
Varme artikler
-
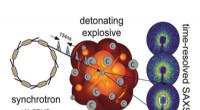 De første amerikanske eksperimenter nogensinde på et nyt røntgenanlæg kan føre til bedre eksplo…Detonationen af kulstofrige højsprængstoffer giver fast kulstof som en hovedbestanddel af produktblandingen, og afhængigt af de termodynamiske forhold bag stødfronten, en række carbonallotroper og -
De første amerikanske eksperimenter nogensinde på et nyt røntgenanlæg kan føre til bedre eksplo…Detonationen af kulstofrige højsprængstoffer giver fast kulstof som en hovedbestanddel af produktblandingen, og afhængigt af de termodynamiske forhold bag stødfronten, en række carbonallotroper og - -
 AI-drevet elektronisk næse til at opsnuse kødets friskhedE-næsen indeholder en stregkode, der ændrer farve på grund af reaktioner med gasser, der udsendes af det henfaldende kød, og en stregkodelæser i form af en smartphone-app drevet af AI, og er blevet tr
AI-drevet elektronisk næse til at opsnuse kødets friskhedE-næsen indeholder en stregkode, der ændrer farve på grund af reaktioner med gasser, der udsendes af det henfaldende kød, og en stregkodelæser i form af en smartphone-app drevet af AI, og er blevet tr -
 Forskere tilbyder overblik over kompositmetalskum og potentielle anvendelserForskere ved North Carolina State University har udviklet en række sammensatte metalskum, der er lettere og stærkere end de materialer, de er lavet af. Skummet kan bruges i applikationer fra rustning
Forskere tilbyder overblik over kompositmetalskum og potentielle anvendelserForskere ved North Carolina State University har udviklet en række sammensatte metalskum, der er lettere og stærkere end de materialer, de er lavet af. Skummet kan bruges i applikationer fra rustning -
 Lab udforsker nye harpikser til lysbaseret 3D-printLLNL -forskere brugte molekylær dynamik (MD) simuleringer til at studere polymerisationen af tre forskellige molekyler fra den samme reaktive gruppe (acrylat), men indeholdende forskellige ikke -rea
Lab udforsker nye harpikser til lysbaseret 3D-printLLNL -forskere brugte molekylær dynamik (MD) simuleringer til at studere polymerisationen af tre forskellige molekyler fra den samme reaktive gruppe (acrylat), men indeholdende forskellige ikke -rea


