Elektronpartal:Nøglen til molekylær geometri
Mærke X Pictures/Stockbyte/Getty Images
Siden introduktionen i 1950'erne har Valence-Shell Electron-Pair Repulsion (VSEPR) modellen været hjørnestenen til at forudsige molekylære former. Princippet er enkelt:elektronpar – både bindinger og ensomme par – frastøder hinanden og arrangerer sig omkring et centralt atom for at maksimere deres adskillelse og derved minimere frastødende energi.
Sådan virker VSEPR
Begynd med en Lewis-punktstruktur for at identificere valenselektronerne for hvert atom. Tæl elektrongrupperne, der omgiver det centrale atom – hvert bindingspar (delte elektroner) og hvert enkelt par (ikke-bindende elektroner). Disse grupper indtager positioner på den ydre skal, så de er så langt fra hinanden som muligt. Det rumlige arrangement af alle disse grupper bestemmer den overordnede geometri; positionerne af de bundne atomer følger det samme arrangement, hvilket giver molekylet dets observerbare form.
Eksempler
Carbondioxid (CO₂) – To bindende par, ingen enlige par. Elektrongrupperne antager et lineært arrangement, så molekylet er lineært.
Vand (H₂O) – Fire elektrongrupper:to bindingspar og to enlige par. De enlige par udøver en større frastødende kraft, komprimerer H–O–H-vinklen og giver et bøjet (V-formet) molekyle.
Ammoniak (NH₃) – Fire elektrongrupper:tre bindingspar og et ensomt par. Det enlige par skubber brintatomerne lidt fra hinanden, hvilket giver en trigonal pyramideform.
Disse klassiske eksempler illustrerer, hvordan antallet og typen af elektronpar dikterer molekylær geometri gennem VSEPR.
 Varme artikler
Varme artikler
-
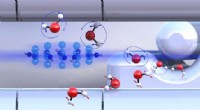 Sammenligning af vandisomerers kemiForsorterede ortho-vand- og para-vand-molekyler med forskelligt orienterede nukleare spins (blå eller røde pile) reagerer med diazenyliumioner (i midten til venstre) ved forskellige hastigheder. Kredi
Sammenligning af vandisomerers kemiForsorterede ortho-vand- og para-vand-molekyler med forskelligt orienterede nukleare spins (blå eller røde pile) reagerer med diazenyliumioner (i midten til venstre) ved forskellige hastigheder. Kredi -
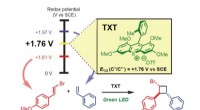 Lys skinner på kemisk produktionsmetodeBilledet illustrerer redoxpotentialet kontrolleret selektiv oxidation af styrener til regio- og stereoselektiv krydsede intermolekylære [2 + 2] cycloaddition via organophotoredox katalyse. Kredit:Yuji
Lys skinner på kemisk produktionsmetodeBilledet illustrerer redoxpotentialet kontrolleret selektiv oxidation af styrener til regio- og stereoselektiv krydsede intermolekylære [2 + 2] cycloaddition via organophotoredox katalyse. Kredit:Yuji -
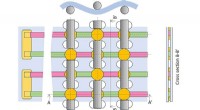 Kropsvarme gennem fleksibelt stof kunne drive IoT-enheder til sundhedsovervågning for mennesker, kæ…Forskere ved Purdue University har skabt en teknologi til at løse tykkelsesproblemet for bærbar strømproduktion. Kredit:Purdue University Bærbar elektronik og andre Internet of Things (IoT) enhede
Kropsvarme gennem fleksibelt stof kunne drive IoT-enheder til sundhedsovervågning for mennesker, kæ…Forskere ved Purdue University har skabt en teknologi til at løse tykkelsesproblemet for bærbar strømproduktion. Kredit:Purdue University Bærbar elektronik og andre Internet of Things (IoT) enhede -
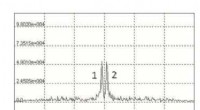 Forskere foreslår en ny metode til at opdage farlige nitrogenholdige væskerNMR -spektrum af mmoniumnitrat. Kredit:Galina Kupriyanova Et team af forskere fra Institut for Fysiske og Matematiske Videnskaber og Informationsteknologier ved Immanuel Kant Baltic Federal Univer
Forskere foreslår en ny metode til at opdage farlige nitrogenholdige væskerNMR -spektrum af mmoniumnitrat. Kredit:Galina Kupriyanova Et team af forskere fra Institut for Fysiske og Matematiske Videnskaber og Informationsteknologier ved Immanuel Kant Baltic Federal Univer
- Fem ting at vide om Elon Musks rumprojekter
- Hubbles majestætiske spiral i Pegasus
- Kunstig intelligens trænet til at analysere årsagssammenhæng
- Hvordan echidna mistede sin gift
- Hvordan kan jeg finde Scorpius -konstellationen på nattehimlen?
- Med en stangmagnet, hvor er styrelinjer det tætteste sammen?


