Sådan tegner du Bohr-diagrammer:En trin-for-trin-vejledning til studerende
Af Jo Jackson | Opdateret 24. marts 2022
Et Bohr-diagram, introduceret af den danske fysiker Niels Bohr i 1913, giver et klart billede af et atoms struktur. Den viser en positivt ladet kerne omgivet af elektroner i koncentriske cirkulære baner, hvor hver bane repræsenterer et særskilt energiniveau. Bohr-diagrammer er ideelle til at undervise i det grundlæggende i kvantemekanik, da de illustrerer, hvordan elektroner optager diskrete energiskaller.
Trin 1 – Indsaml elementoplysninger
Se det periodiske system for at identificere det element, du ønsker at repræsentere. Registrer dets atomnummer (antallet af protoner) og massetal (protoner plus neutroner). I et neutralt atom er antallet af elektroner lig med antallet af protoner. Bemærk elementets periode:elementer i første række har ét energiniveau, dem i anden række har to, og så videre.
Trin 2 – Afbild kernen
Tegn en lille cirkel til kernen. Indeni skal du skrive elementets symbol og angive antallet af protoner og neutroner. Omring denne kerne med en eller flere ringe, der hver svarer til et forskelligt energiniveau baseret på elementets periode.
Trin 3 – Placer elektronerne
Marker elektroner som prikker på ringene. Hvert energiniveau har en kapacitet:Den første (indre) skal rummer op til 2 elektroner, den anden op til 8, den tredje op til 18 og den fjerde op til 32. Når elektronerne er placeret, er diagrammet komplet.
Sidste artikelTrin-for-trin guide til produktion af bæredygtig biogas
Næste artikelTre vigtige ligheder mellem elementer og forbindelser
 Varme artikler
Varme artikler
-
 Supraballs tilbyder en ny måde at farve materialer påEt billede af en regnbuelignende blomster, malet med supraball blæk lavet af fem forskellige størrelser af kerne-skal syntetiske melanin nanopartikler. Kredit:Ming Xiao, Universitetet i Akron Et i
Supraballs tilbyder en ny måde at farve materialer påEt billede af en regnbuelignende blomster, malet med supraball blæk lavet af fem forskellige størrelser af kerne-skal syntetiske melanin nanopartikler. Kredit:Ming Xiao, Universitetet i Akron Et i -
 Polymerprofessor udvikler sikrere komponent til lithiumbatterierEn solid polymer elektrolytfilm, der bliver brugt i lithiumbatterier i forskningen ledet af Dr. Yu Zhu. Kredit:University of Akron Strømkilden til implanteret medicinsk udstyr, elbiler, ubemandede
Polymerprofessor udvikler sikrere komponent til lithiumbatterierEn solid polymer elektrolytfilm, der bliver brugt i lithiumbatterier i forskningen ledet af Dr. Yu Zhu. Kredit:University of Akron Strømkilden til implanteret medicinsk udstyr, elbiler, ubemandede -
 Web-baseret open source-program bestemmer proteinstrukturerStefan Arold (th.) og hans team spiller en afgørende rolle i det lokale videnskabelige samfund gennem samarbejde med andre forskningsgrupper i Kongeriget. Kredit:KAUST ContaMiner er en webbaseret,
Web-baseret open source-program bestemmer proteinstrukturerStefan Arold (th.) og hans team spiller en afgørende rolle i det lokale videnskabelige samfund gennem samarbejde med andre forskningsgrupper i Kongeriget. Kredit:KAUST ContaMiner er en webbaseret, -
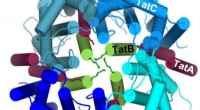 Biokemikere undersøger transporten af store proteiner gennem bakterielle cellemembranerFire TatC-molekyler (blå) danner en cirkel omkring fire TatB-molekyler (grøn) for at danne et hulrum i midten, hvori det protein, der skal transporteres, kan indsættes nedefra. Kredit: Journal of Biol
Biokemikere undersøger transporten af store proteiner gennem bakterielle cellemembranerFire TatC-molekyler (blå) danner en cirkel omkring fire TatB-molekyler (grøn) for at danne et hulrum i midten, hvori det protein, der skal transporteres, kan indsættes nedefra. Kredit: Journal of Biol
- Hvad er 450 gram lige i ounces?
- Billede:Farverne i Saturns ringe
- Når en væske er fuld op med opløst fast stof, så er denne opløsning?
- Flashtørke bringer støv og frygt til sydlige bønder
- Amazonas skovrydning og antallet af brande viser, at sommeren 2019 ikke er et normalt år
- Over 300 millioner unge mennesker har oplevet online seksuelt misbrug, udnyttelse, finder metastudie…


