Tre vigtige ligheder mellem elementer og forbindelser
Af Mariecor Agravante | Opdateret 24. marts 2022
vchal/iStock/GettyImages
Ved første øjekast kan grundstoffer og forbindelser virke adskilte, men alligevel deler de kerneligheder, der understreger stoffets struktur. Begge er sammensat af atomer, holdt sammen af kemiske bindinger, og hver eksisterer som et rent, homogent stof.
Grundlæggende stofenhed:Atomet
Atomet er den grundlæggende byggesten i stof. Når atomer kombineres, danner de molekyler. Der findes to hovedmolekylære typer:grundstoffer - molekyler af en enkelt atomart - og forbindelser - molekyler sammensat af to eller flere forskellige atomer. For eksempel består elementært guld (Au) udelukkende af guldatomer, mens vand (H2O) kombinerer brint og oxygen.
Bånder, der holder atomer sammen
Stabilitet i både grundstoffer og forbindelser opstår fra interatomiske bindinger. De primære bindingstyper er kovalente, hvor elektroner deles, og ioniske, hvor elektroner overføres og skaber modsat ladede ioner, der tiltrækker. Det diatomiske oxygenmolekyle (O₂) stabiliseres af en kovalent binding, hvorimod almindeligt salt (NaCl) er afhængig af en ionbinding mellem Na+ og Cl⁻. Selv ædelgasser, normalt inerte, kan danne forbigående bindinger under excitation - en proces kendt som dimerisering - og producerer laboratorieforbindelser såsom xenonhexafluorplatinat (XePtF₆) og xenondioxid (XeO₂).
Rene stoffer efter definition
Renhed betyder, at et stof ikke kan nedbrydes uden at ændre dets væsentlige egenskaber. Grundstoffer opfylder dette kriterium, fordi de kun består af én atomart. Forbindelser er rene, fordi hvert molekyle er identisk; nedbrydning af en forbindelse giver dens konstituerende atomer eller grundstoffer, som har forskellige egenskaber.
Homogenitet på tværs af hele stoffet
Homogene materialer udviser ensartet sammensætning og udseende overalt. En ren sølvplade indeholder for eksempel kun sølvatomer og viser de karakteristiske egenskaber af sølv overalt. I modsætning hertil er en rusten tinoverflade heterogen. På samme måde er rent vand homogent; kontaminering introducerer heterogenitet. Således bevarer både rene grundstoffer og rene forbindelser ensartede egenskaber i deres helhed.
 Varme artikler
Varme artikler
-
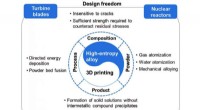 Forskere gennemgår fremskridt inden for 3D-print af højentropi-legeringerOversigt over forholdet mellem HEAer og 3D-print, med hensyn til kompositionsdesignet, pulver udvikling, trykprocesser, produkt egenskaber, og potentielle applikationer. Kredit:SUTD Højentropi-leg
Forskere gennemgår fremskridt inden for 3D-print af højentropi-legeringerOversigt over forholdet mellem HEAer og 3D-print, med hensyn til kompositionsdesignet, pulver udvikling, trykprocesser, produkt egenskaber, og potentielle applikationer. Kredit:SUTD Højentropi-leg -
 Vand var en vinder i opsamling af kuldioxidTESET, før og efter vandbehandling. Vandet har ændret strukturen i materialet. Kredit:Kenneth P. Mineart, NCSU Klimabekymringer går hånd i hånd med CO 2 emissioner bekymringer. Emissionerne ramt
Vand var en vinder i opsamling af kuldioxidTESET, før og efter vandbehandling. Vandet har ændret strukturen i materialet. Kredit:Kenneth P. Mineart, NCSU Klimabekymringer går hånd i hånd med CO 2 emissioner bekymringer. Emissionerne ramt -
 Kantarelsvampe som smagsforstærkerDr. Verena Mittermeier fra formanden for fødevarekemi og molekylær sensorisk videnskab og Andreas Dunkel fra Leibniz-instituttet for fødevaresystembiologi foran deres institut. Kredit:Leibniz-LSB@TUM
Kantarelsvampe som smagsforstærkerDr. Verena Mittermeier fra formanden for fødevarekemi og molekylær sensorisk videnskab og Andreas Dunkel fra Leibniz-instituttet for fødevaresystembiologi foran deres institut. Kredit:Leibniz-LSB@TUM -
 Lab træder på gassen for at forbedre kemisk produktionIn situ og ex situ røntgenfotoelektronspektroskopi og elektronmikroskopi afslører stabiliteten af nikkelkobberlegeringskatalysatorer til ikke-oxidativ ethanoldehydrogenering forbedres ved at generer
Lab træder på gassen for at forbedre kemisk produktionIn situ og ex situ røntgenfotoelektronspektroskopi og elektronmikroskopi afslører stabiliteten af nikkelkobberlegeringskatalysatorer til ikke-oxidativ ethanoldehydrogenering forbedres ved at generer
- Billede:Skovbrande, der løber amok i Californien
- Ny forskning identificerer tredobbelt problemer for mangrove-kyster
- Er et mineral er et naturligt organisk fast stof, der er dannet i jorden sand eller falsk?
- Hvad er par af kræfter?
- Nedlukninger og forskning:Hvad vi mistede, og hvad vi står til at vinde
- AAAS-panelet fokuserer på køreplanen til radikal transformation af AI-forskningsvirksomheden


