Model a Calcium Atom:En simpel guide til begyndere
Af Kevin Beck Opdateret 24. marts 2022
Atomet er den mindste stofenhed, der bevarer egenskaberne af en større helhed. Det er ikke udeleligt, men stykker af atomer, især "klumperne" af nukleare komponenter kaldet kvarker , er egentlig kun gode til at lave atomer. Forskellige slags atomer kaldes grundstoffer, hvoraf næsten 120 (92 af dem naturligt forekommende) er kendt.
Det meste stof består af flere slags atomer, arrangeret i grupper på to eller flere og har specifikke formler; to eller flere atomer, der er kemisk bundet sammen, udgør et molekyle. For eksempel har et vandmolekyle formlen H2O, hvilket betyder, at det er lavet af grundstofferne hydrogen (H) og oxygen (O) i et atom- eller molforhold på 2 til 1.
Calcium er et velkendt element, der er afgørende for god knoglesundhed og andre funktioner i den menneskelige krop. Calciumatomet er hverken et lille eller et særligt besværligt atom, hvilket gør det til en god kandidat til at bygge et tredimensionelt atommodelprojekt for at illustrere de fremtrædende punkter i denne struktur.
Atomet:Grundlæggende
Atomet:Grundlæggende
Atomer består af lige mange protoner og elektroner i deres grundlæggende (ikke-ioniserede) tilstand, nummereret fra en til 118 fra 2020. Antallet af protoner, atomnummeret, definerer grundstoffet. Alle grundstoffer undtagen brint har også en eller flere neutroner; protoner og neutroner er omtrent lige store (i størrelsesordenen 10-27 kg), mens elektroner er næsten 2.000 gange mindre.
Antallet af protoner og neutroner er nogenlunde det samme, selvom når du bevæger dig opad gennem grundstoffernes periodiske system, begynder neutroner at være synligt flere end protoner i de fleste atomer. Varianter af grundstoffer, der kun adskiller sig i neutrontal, kaldes isotoper .
De negativt ladede elektroner optager rum langt, langt fra protonen, i det mindste på skalaen af et atom, som kun er omkring 1 × 10−10 m på tværs. Disse findes i energiniveauer eller skaller, som for mange atomer omfatter underskaller . Subshells indeholder igen orbitaler , som hver kan rumme op til to elektroner.
Hver række i det periodiske system repræsenterer en skal, hvor antallet af elektroner en skal kan indeholde er to, otte, otte og 18 i de første fire rækker af det periodiske system.
Calcium 3D Model Atom
Calcium 3D Model Atom
Du kan se fra det periodiske system, at calcium har et atomnummer på 20 og en atommasse på 40,78 dalton. Det betyder, at grundstoffets mest stabile isotop har 20 neutroner (40 − 20). Du kan vælge grønne kugler til at repræsentere protoner og orange kugler af lignende størrelse til at repræsentere neutroner, og mindre gule kugler eller kugler til at repræsentere elektroner.
Du kan arrangere dine "protoner" og "neutroner" i en kuglelignende kerne, måske lime dem sammen og derefter beslutte, hvordan du skal arrangere dine elektroner.
Fra tabellen kan du se, at calcium har to elektroner i den første skal (begge i det, der kaldes 1s subshell), otte i den anden shell (2 i 2s subshell, 6 i 2p subshell), otte i den tredje skal (2 i 3s subshell, 3 i 3p subshell) og to i den fjerde skal. Disse er calciums valens eller kemisk reaktive elektroner.
Se forskellige onlinereferencer for at se, hvordan elektronunderskaller er afbildet i 3D-rum. Du kan tegne et calciumatomdiagram til at ledsage din model, så det dækker enhver information, du kan finde vanskelig at præsentere visuelt.
Yderligere atomer til modellering
Yderligere atomer til modellering
En neonatommodel kunne f.eks. gøre seerne bekendt med begrebet ædelgasser og fuldvalensskaller, eller en natriumatommodel kunne tjene som et repræsentativt simpelt metal, der binder til halogener såsom klor.
Sidste artikelForstå tonicitet:osmose og isotoniske løsninger
Næste artikelForståelse af parallellogrammer:typer, egenskaber og eksempler
 Varme artikler
Varme artikler
-
 Video:Sådan spotter du falske metaller med syrerKredit:The American Chemical Society Syrer er reaktive, med selv svage syrer som eddike, der interagerer med andre materialer for at imponere eleverne. Men stærke syrer kan virkelig vise sig. For
Video:Sådan spotter du falske metaller med syrerKredit:The American Chemical Society Syrer er reaktive, med selv svage syrer som eddike, der interagerer med andre materialer for at imponere eleverne. Men stærke syrer kan virkelig vise sig. For -
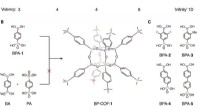 Ny kovalent organisk ramme, der bruger bor og fosfor, giver mulighed for bedre tilslutningHøjere valens i COFer og syntetisk strategi for polycubaner. (A) Bygningsenheder med valens 3 og 4 bruges i øjeblikket i design og syntese af 3D COFer; terninger med valens på 8 og uendelige 1D-stænge
Ny kovalent organisk ramme, der bruger bor og fosfor, giver mulighed for bedre tilslutningHøjere valens i COFer og syntetisk strategi for polycubaner. (A) Bygningsenheder med valens 3 og 4 bruges i øjeblikket i design og syntese af 3D COFer; terninger med valens på 8 og uendelige 1D-stænge -
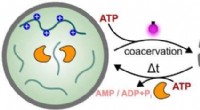 Hvordan lys kan bruges til at styre processer i syntetiske cellerKredit:Shoupeng Cao et al., Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202205266 Syntetiske (kunstigt producerede) celler kan efterligne visse funktioner af biologiske celler.
Hvordan lys kan bruges til at styre processer i syntetiske cellerKredit:Shoupeng Cao et al., Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202205266 Syntetiske (kunstigt producerede) celler kan efterligne visse funktioner af biologiske celler. -
 Genanvendelse af dimethyloxalylglycin til at hæmme glutaminmetabolismeKredit:CC0 Public Domain Et team af forskere fra Storbritannien og USA har fundet ud af, at et lægemiddel, der bruges til at studere hypoxi, også kan bruges til at hæmme glutaminmetabolisme - et m
Genanvendelse af dimethyloxalylglycin til at hæmme glutaminmetabolismeKredit:CC0 Public Domain Et team af forskere fra Storbritannien og USA har fundet ud af, at et lægemiddel, der bruges til at studere hypoxi, også kan bruges til at hæmme glutaminmetabolisme - et m
- Hvad sker der, når ilt er det blandet med vand?
- Forskerhold finder en måde at nøjagtigt måle permeabiliteten af kulstofnanorør
- I hvilke bindinger er den kemiske energi, der er opbevaret i fedt og kulhydrater?
- Hvilket økosystem er en manatee del af?
- Hvor findes den tempererede løvskov i Canada?
- Sådan fungerer hjernevask


