Sådan bestemmes antallet af atomer i et kemisk grundstof
Af Chris Deziel Opdateret 24. marts 2022
ktsimage/iStock/GettyImages
Et atom er et grundstof. De to ord er synonyme, så hvis du leder efter antallet af atomer i et grundstof, er svaret altid ét og kun ét. Forskere kender til 118 forskellige grundstoffer, som de kategoriserer i det periodiske system, et diagram, der arrangerer dem i stigende rækkefølge efter antallet af protoner i deres kerner. Dette arrangement giver dig mulighed for at besvare et væsentligt spørgsmål med et øjeblik:"Hvad er antallet af protoner i et bestemt element?" For at svare på det skal du blot se på den plads, elementet indtager i diagrammet. Stednummeret svarer til antallet af protoner.
TL;DR (for lang; læste ikke)
Hvis du har en prøve, der indeholder atomer af et enkelt grundstof, kan du finde antallet af atomer ved at veje det.
Elementer, der danner diatomiske molekyler
Elementer, der danner diatomiske molekyler
Nogle atomer kan danne kovalente bindinger med andre atomer af samme grundstof for at danne diatomiske molekyler. Den bedst kendte er oxygen (O). Et enkelt oxygenatom er meget reaktivt, men når det danner en binding med et andet oxygenatom for at danne O2, er kombinationen mere stabil. Dette er den form, hvor ilt findes i jordens atmosfære. Fire andre elementer kan kombineres på denne måde ved standard temperatur og tryk. De omfatter nitrogen (N), som er det mest udbredte grundstof i atmosfæren, brint (H), klor (Cl) og fluor (F). To andre grundstoffer, brom (Br) og jod (I), kan danne diatomiske molekyler ved højere temperaturer. Alle diatomiske molekyler indeholder to atomer.
Ædelgasser og metaller
Ædelgasser og metaller
Nogle atomer, såsom natrium og fosfor, er så reaktive, at de aldrig findes frie i naturen. Imidlertid er to grupper af grundstoffer, ædelgasser og ædelmetaller, stabile og kan eksistere i prøver, der kun indeholder ikke-bundne atomer af det pågældende grundstof. For eksempel indeholder en beholder fuld af argongas (Ar) kun argonatomer, og en bar med rent guld indeholder kun guldatomer (Au). Hvis du har en stor prøve af en ædelgas eller metal, kan du beregne, hvor mange atomer det indeholder ved at veje det.
Ud over disse gasser og metaller kan kulstof (C) også eksistere i fri tilstand. Diamant og grafit er de to mest almindelige former. Blandt ikke-metaller er kulstof enestående i sin evne til at eksistere på denne måde.
Tælle atomer
Tælle atomer
For at beregne antallet af atomer i en prøve skal du finde ud af, hvor mange mol af grundstoffet prøven indeholder. En muldvarp er en enhed kemikere bruger. Det er lig med Avogadros antal (6,02 X 1023) atomer. Per definition er vægten af et mol af et grundstof (dets molære masse) lig med dets atomvægt i gram. Atomvægten for hvert grundstof er på det periodiske system lige under grundstoffets symbol. Atomvægten af kulstof er 12 atommasseenheder (amu), så vægten af en mol er 12 gram.
Hvis du har en prøve, der kun indeholder atomer af et bestemt grundstof, skal du veje prøven i gram og dividere med grundstoffets atomvægt. Kvotienten fortæller dig antallet af mol. Gang det med Avogadros tal, og du vil finde ud af, hvor mange atomer prøven indeholder.
Eksempler
Eksempler
1\. Hvor mange atomer er der i en ounce rent guld?
En ounce er 28 gram, og guldets atomvægt er 197. Prøven indeholder 28 ÷ 197 =0,14 mol. Hvis du multiplicerer dette med Avogadros tal, fortæller du antallet af atomer i prøven =8,43 x 1022 atomer.
2\. Hvor mange oxygenatomer er der i en gasprøve, der vejer 20 gram?
Samme procedure gælder for at finde antallet af atomer i en diatomisk gas, selvom atomerne er gået sammen og dannet molekyler. Atomvægten af oxygen er 16, så en mol vejer 16 gram. Prøven vejer 20 gram, hvilket svarer til 1,25 mol. Derfor er antallet af atomer 7,53 x 1023.
 Varme artikler
Varme artikler
-
 Nøjagtig pumpeflowhastighed:Trin-for-trin guide til måling af gallons pr. minutAf William Hirsch Opdateret 24. marts 2022 Hvis du spekulerer på, hvor mange liter væske per minut din pumpe er i stand til at bevæge sig, kan du udføre dette hurtige eksperiment for at finde ud af
Nøjagtig pumpeflowhastighed:Trin-for-trin guide til måling af gallons pr. minutAf William Hirsch Opdateret 24. marts 2022 Hvis du spekulerer på, hvor mange liter væske per minut din pumpe er i stand til at bevæge sig, kan du udføre dette hurtige eksperiment for at finde ud af -
 Programmerbar dråbe manipulation med en magnetisk aktiverings robotTypisk adfærd for dråberne manipuleret ved hjælp af den magnetisk aktiverede robot. Kredit:Science Advances, doi:10.1126/sciadv.aay5808 Dråbe manipulation i materialevidenskab kan bidrage til vand
Programmerbar dråbe manipulation med en magnetisk aktiverings robotTypisk adfærd for dråberne manipuleret ved hjælp af den magnetisk aktiverede robot. Kredit:Science Advances, doi:10.1126/sciadv.aay5808 Dråbe manipulation i materialevidenskab kan bidrage til vand -
 Mere sund mælkechokolade ved at tilføje jordnødder, kaffespildKredit:CC0 Public Domain Mælkechokolade er en forbrugerfavorit verden over, værdsat for sin søde smag og cremede tekstur. Denne konfekt kan findes i alle typer godbidder, men det er ikke ligefrem
Mere sund mælkechokolade ved at tilføje jordnødder, kaffespildKredit:CC0 Public Domain Mælkechokolade er en forbrugerfavorit verden over, værdsat for sin søde smag og cremede tekstur. Denne konfekt kan findes i alle typer godbidder, men det er ikke ligefrem -
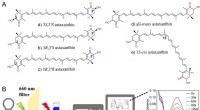 Forskelle fundet i antioxidantaktiviteter af astaxanthinisomerer mod singlet oxygen(A) Strukturer af stereoisomerer af astaxanthin. (B) Måling af singlet-iltslukningskapaciteten af antioxidanter. Kredit:Zheng Xinxin For nylig foreslog forskere ledet af prof. Huang Qing fra Inst
Forskelle fundet i antioxidantaktiviteter af astaxanthinisomerer mod singlet oxygen(A) Strukturer af stereoisomerer af astaxanthin. (B) Måling af singlet-iltslukningskapaciteten af antioxidanter. Kredit:Zheng Xinxin For nylig foreslog forskere ledet af prof. Huang Qing fra Inst
- Hvad er den astronomiske enhed med orbital hastighed?
- Afgiver solen korte eller lange bølgelængder?
- EXPLAINER:Hvorfor gensøger skoler talentuddannelse?
- Krydsord på atomisotoper og elektronisk struktur?
- Sammenlign geologisk tid med kolonne?
- Opdagelse af afgrødegener kommer til roden af fødevaresikkerhed


