Beregning af fortynding:Volumen af NaOH nødvendig for en 0,10 M opløsning
1. Forstå Molaritet
* Molaritet (M) er et mål for koncentration, der repræsenterer mol opløst stof pr. liter opløsning.
2. Opsæt ligningen
Vi kan bruge følgende ligning:
M1V1 =M2V2
hvor:
* M1 =Molaritet af den koncentrerede opløsning (6,0 M NaOH)
* V₁ =Volumen af den koncentrerede opløsning (det vi ønsker at finde)
* M₂ =Molaritet af den fortyndede opløsning (0,10 M NaOH)
* V₂ =Volumen af den fortyndede opløsning (1,0 L)
3. Løs for V₁
* Omarranger ligningen for at løse for V₁:
V1 =(M2V2)/M1
* Erstat værdierne:
V1 =(0,10 M * 1,0 L) / 6,0 M
* Beregn:
V1 =0,017 L
4. Konverter til Milliliter
* Da 1 liter (L) =1000 milliliter (mL):
V1 =0,017 L * 1000 mL/L =17 mL
Svar: Du skal bruge 17 milliliter 6,0 M NaOH for at fremstille 1,0 liter 0,10 M NaOH-opløsning.
Sidste artikelKonverter milligram til centigram:En simpel guide
Næste artikelEn funktion udfører en beregning, der resulterer i?
 Varme artikler
Varme artikler
-
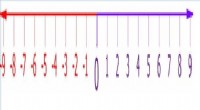 Mestring af tallinjer:En praktisk vejledning til undervisning i addition, subtraktion og mereAf Andrea Hermitt, Opdateret 30. august 2022 Tallinjer er et kraftfuldt visuelt værktøj, der hjælper eleverne med at forstå grundlæggende aritmetiske operationer. Ved fysisk at bevæge sig langs en li
Mestring af tallinjer:En praktisk vejledning til undervisning i addition, subtraktion og mereAf Andrea Hermitt, Opdateret 30. august 2022 Tallinjer er et kraftfuldt visuelt værktøj, der hjælper eleverne med at forstå grundlæggende aritmetiske operationer. Ved fysisk at bevæge sig langs en li -
 Sådan bruger du TI‑84-beregneren til at tilføje logaritmerAf Carl Raimer • Opdateret 30. august 2022 En logaritme (log) er det inverse af eksponentiering. Selvom enhver base kan bruges, håndterer TI-84-beregneren base-10 (log) og naturlig logaritme (ln) ind
Sådan bruger du TI‑84-beregneren til at tilføje logaritmerAf Carl Raimer • Opdateret 30. august 2022 En logaritme (log) er det inverse af eksponentiering. Selvom enhver base kan bruges, håndterer TI-84-beregneren base-10 (log) og naturlig logaritme (ln) ind -
 Sådan beregnes varians på en TI-84 grafregnerEugene Mymrin/Getty Images Varians måler, hvordan dataværdier spredes omkring middelværdien. Med en TI‑84 grafregner kan du beregne variansen øjeblikkeligt ved først at opnå standardafvigelsen (SD) o
Sådan beregnes varians på en TI-84 grafregnerEugene Mymrin/Getty Images Varians måler, hvordan dataværdier spredes omkring middelværdien. Med en TI‑84 grafregner kan du beregne variansen øjeblikkeligt ved først at opnå standardafvigelsen (SD) o -
 Menneskelige virkninger af kulstofemissioner:Klimarisici og tilpasningMedioimages/Photodisc/Photodisc/Getty Images Kulstofemissioner er den primære drivkraft for klimaændringer, hvor kuldioxid tegner sig for over 80% af de amerikanske drivhusgasser, ifølge Environmenta
Menneskelige virkninger af kulstofemissioner:Klimarisici og tilpasningMedioimages/Photodisc/Photodisc/Getty Images Kulstofemissioner er den primære drivkraft for klimaændringer, hvor kuldioxid tegner sig for over 80% af de amerikanske drivhusgasser, ifølge Environmenta
- Den lave tæthed af nogle exoplaneter er bekræftet
- Nære familier, der bedre kan klare økonomisk usikkerhed, siger ny forskning
- Hvad er grundstofferne i det periodiske system baseret på?
- Gamle menneskelige forstyrrelser kan skævvride forståelsen af Amazon og dens indvirkning (Opdate…
- Er naturgas håndgribelig eller ej?
- El Niño kunne skubbe den globale opvarmning forbi 1,5 C - men hvad er det, og hvordan påvirker det…


